Минералы. Справочник. Том 1. Самородные элементы, интерметаллические соединения, карбиды, нитриды, фосфиды, арсениды, антимониды, висмутиды, сульфиды, селениды, теллуриды.
Редактор(ы):Бонштедт-Куплетская Э.М., Чухров Ф.В.
Издание:Издательство Академии наук СССР, Москва, 1960 г., 617 стр.
Предлагаемый вниманию читателей справочник «Минералы» является первым полным минералогическим справочником, составленным в СССР. При подготовке его обращено внимание на возможно более широкое использование данных новейшей советской и иностранной литературы с тем, чтобы дать читателю представление о современном состоянии изученности отдельных минералов.
В наше время, когда для характеристики минералов используются данные сопредельных наук — физики, химии и др., составление полного минералогического справочника представляет большие трудности; некоторые свойства (например, магнитные, электрические и др.) в литературе охарактеризованы лишь для немногих минералов.
В отличие от распространенного среди минералогов 7-го издания «Системы минералогии» Дана, предлагаемый справочник в ряде разделов преимущественно базируется на достижениях отечественной минералогии. В дополнение к данным, содержащимся в других минералогических справочниках, в настоящем справочнике приведены межплоскостные расстояния, результаты термического анализа и некоторые другие сведения, необходимые для диагностики минералов.
В основу справочника легли классические русские и иностранные сводки п справочникп, список которых приведен ниже. Более новые сведения о минералах заимствованы из периодических изданий, монографий п сводок последних пет.
Справочник предназначен для минералогов, геохимиков, петрографов, геологов различных специальностей и всех лиц, имеющих дело с изучением, добычей и практическим использованием минералов.
Справочник «Минералы» намечено издать в семи томах. Принято следующее распределение материала по томам:I том — Самородные элементы.
 Из данных морфологической кристаллографии указывается отношение осей, приводится список наиболее распространенных форм с указанием их сферических угловых координат (з и р) и наиболее характерных меж-грапных углов, перечисляются формы второстепенного значения.Морфологическая установка, как правило, не приведена к рентгеновской (предпочтительно принималась морфологическая установка, которой отвечает наименьшая сумма цифр символов главных форм минерала). При расхождении рентгеновского (а0: су с0) и морфологического (а : Ъ : с) отношений осей обе установки сопоставляются; для минералов, морфологические установки которых менялись, дано сопоставление символов главных форм для различных установок и приведены формулы перехода *.Символы граней, направление спайности и оптическая ориентировка в дальнейшем тексте во всех случаях даны в принятой, морфологической установке.На прилагаемых чертежах кристаллов, взятых из оригинальных статей и из справочников, буквенные обозначения во многих случаях изменены в соответствии с буквами, указанными при перечислении форм (в основном приняты буквенные обозначения по Дана).
Из данных морфологической кристаллографии указывается отношение осей, приводится список наиболее распространенных форм с указанием их сферических угловых координат (з и р) и наиболее характерных меж-грапных углов, перечисляются формы второстепенного значения.Морфологическая установка, как правило, не приведена к рентгеновской (предпочтительно принималась морфологическая установка, которой отвечает наименьшая сумма цифр символов главных форм минерала). При расхождении рентгеновского (а0: су с0) и морфологического (а : Ъ : с) отношений осей обе установки сопоставляются; для минералов, морфологические установки которых менялись, дано сопоставление символов главных форм для различных установок и приведены формулы перехода *.Символы граней, направление спайности и оптическая ориентировка в дальнейшем тексте во всех случаях даны в принятой, морфологической установке.На прилагаемых чертежах кристаллов, взятых из оригинальных статей и из справочников, буквенные обозначения во многих случаях изменены в соответствии с буквами, указанными при перечислении форм (в основном приняты буквенные обозначения по Дана).
 Для минералов моноклинной сингоний, кристаллы которых удлинены по оси Ъ (группа эпидота и др.), помимо вир, приводятся ера и ра, отвечающие вертикальному направлению оси Ъ, необходимые для измерений кристаллов такого типа.
Для минералов моноклинной сингоний, кристаллы которых удлинены по оси Ъ (группа эпидота и др.), помимо вир, приводятся ера и ра, отвечающие вертикальному направлению оси Ъ, необходимые для измерений кристаллов такого типа.Арсениды – Справочник химика 21
В качестве солеподобных соединений, в которых мышьяк, сурьма и висмут проявляют степень окисления —3, можно рассматривать арсениды, стибиды (антимониды) и висмутиды s-элементов I и II групп (КзЭ, СадЭа, М зЭ,2 и др.). В большинстве же других случаев при взаимодействии металлов с мышьяком, сурьмой и висмутом образуются соединения металлического типа. Стибиды и арсениды / -элементов и элементов подгруппы цинка — полупроводники. В ряду однотипных нитридов, фосфидов, арсенидов, стибидов и висмутидов ширина запрещенной зоны уменьшается, что свидетельствует об увеличении доли нелокализованной связи. НапримерСоставьте формулы соединений по их названиям оксид меди (I), нитрид кальция, арсенид натрия, сернистая кислота, гидроксид хрома (II), сульфид олова (I ).
 [c.40]
[c.40]Пниктогениды. К пниктогенидам относятся нитриды, фосфиды, арсениды и стибиды — соединения со степенью окисления элемента V главной подгруппы —3. В силу более высокой электроотрицательности и наименьшего радиуса атома азота среди нниктогенидов нитриды по своему составу и свойствам отличаются от производных фосфора, мышьяка и сурьмы, которые имеют и меньшее практическое значение. [c.342]
Кристалл арсенида галлии имеет алмазоподобную структуру. Определить тип и механизм гибридизации орбиталей в атомах галлия и мышьяка и характер образующейся связи. [c.57]
Широкое распространение получили полупроводниковые соединения. Такие соединения образуются, например, элементами пятой и третьей групп периодической системы, из них большое значение имеет арсенид галлия ОаАз. Ширина запрещенной зоны в подобных соединениях обычно растет со степенью ионности связи и определяется поэтому разницей электроотрицательностей составляющих их атомов. Замещение атомов соединения на атомы примесей с отличными валентностями приводит, как и в случае германия, к п- (например, при замене Аз в ОаАз на атом селена или теллура) или к р-проводимости (например, при замене в том же соединении Оа на Са или Mg).
Замещение атомов соединения на атомы примесей с отличными валентностями приводит, как и в случае германия, к п- (например, при замене Аз в ОаАз на атом селена или теллура) или к р-проводимости (например, при замене в том же соединении Оа на Са или Mg).
Водородные соединения элементов подгруппы азота общей формулы ЭНз представляют собой бесцветные газообразные вещества с характерными резкими запахами. Непосредственным синтезом из элементов получить гидриды азота и его аналогов довольно трудно, их обычно получают путем разложения соответствующих нитридов, фосфидов или арсенидов металлов водой [c.80]
Образуются НдЭ действием разбавленных кислот на арсениды, стибиды и висмутиды [c.382]
Арсенид никеля — минерал никелевый колчедан, никелин, т. пл. 968 °С. [c.570]
Сходным образом небольшие количества оксида мышьяка ускоряют коррозию стали в кислотах (например, в НаЗО ), возможно, благодаря формированию арсенидов.
Пленки высокоупорядоченного углерода С-60 можно легко наращивать на кристаллических подложках, таких как арсенид галлия. Это свойство открывает возможность использования таких пленок в производстве микроэлектронных устройств, [c.14]
Развитие исследований и разработок графита для атомной промышленности вылилось в ряд других практических следствий. К их числу следует отнести использование высокочистых углеграфитовых материалов для тиглей, нагревателей, форм для производства полупроводниковых кремния, германия, арсенида галия.  14]
14]
Водородный электрод нельзя применять в присутствии легко окисляющихся или восстанавливающихся веществ, например, солей азотной, хромовой, марганцовой кислот, закиси железа и органических соединений, а также веществ, отравляющих поверхность платины (т. е. вытесняющих из иее водород). К ним принадлежат свободные галогены, арсениды, сульфиды и др. При соединении водородного электрода с другими электродами следует применять электролитический мостик. [c.158]
Многие вещества с тетраэдрическими связями — полупроводники. Они представляют большой интерес как материал для выпрямителей переменного тока, усилителей, фотоэлементов, датчиков, термоэлектрических генераторов и др. Многие из них успешно конкурируют с полупроводниковыми германием и кремнием. На основе InSb работают приборы, сигнализирующие о появлении нагретого тела на большом расстоянии. Арсенид галлия GaAs более перспективен, чем Si, в солнечных батареях. [c.202]
В твердотельных лазерах в качестве активной среды используют как диэлектрики (рубин, стекло с добавками неодима, алюмоиттрие-вый гранат – АИГ), так и полупроводники (например, арсенид галлия). В газовых лазерах активной фазой могут быть чистые газы (Вг, N6, Кг, Хе) или смеси газов (Не – N6, С02-Н2 Не). К.п.д. твердотельных лазеров лежит в пределах 0,01-4%, а газовых 8-30%, причем наиболь- [c.97]
В газовых лазерах активной фазой могут быть чистые газы (Вг, N6, Кг, Хе) или смеси газов (Не – N6, С02-Н2 Не). К.п.д. твердотельных лазеров лежит в пределах 0,01-4%, а газовых 8-30%, причем наиболь- [c.97]
Для определения микропрцмесей в арсениде галлия применяют два способа концентрирования. Сначала отгоняют основной компонент в виде АзВг , при этом происходит относительное концентрирование (увеличивается соотношение между микрокомпонентами и основным компонентом). Далее путей соосаждения с коллектором проводят абсолютное концентрирование микро-компонентов. Сочетание двух методов концентрирования позволяет добиться высокого значения коэффициента концентрирования. [c.315]
Соединения галлия Ga и индия In с неметаллами V и VI групп служат основой многих современных полупроводниковых материалов (например, арсенид галлия GaAs, антимонид индия 1п8Ь). [c.152]
Монокристаллы германия, кремния, арсенида галлия, сульфида свинца и т. п. используют для изготовления полупроводниковой аппаратуры диодов, триодов и т. д. (см. разд. У.14). Монокристаллы рубина, фторида лития и некоторые полупроводники применяются в лазерах. Монокристаллы кварца, каменной соли, кремния, германия, исландского шпата, фторида лития и др. применяют в оптических узлах многих приборов физико-химического анализа. Монокристаллы кварца и сегиетовой соли используют для стабилизации радиочастот, генерирования ультразвука, изготовления основных деталей микрофонов, телефонов, манометров, адаптеров и т. д. Монокристаллы алмаза широко используются при обработке особо твердых материалов и бурении горных пород. Отходы монокристаллов рубина нашли применение в часовой промышленности. Многие монокристаллы применяются так же в качестве украшений (бриллиант, топаз, сапфир, рубин и др.). [c.38]
п. используют для изготовления полупроводниковой аппаратуры диодов, триодов и т. д. (см. разд. У.14). Монокристаллы рубина, фторида лития и некоторые полупроводники применяются в лазерах. Монокристаллы кварца, каменной соли, кремния, германия, исландского шпата, фторида лития и др. применяют в оптических узлах многих приборов физико-химического анализа. Монокристаллы кварца и сегиетовой соли используют для стабилизации радиочастот, генерирования ультразвука, изготовления основных деталей микрофонов, телефонов, манометров, адаптеров и т. д. Монокристаллы алмаза широко используются при обработке особо твердых материалов и бурении горных пород. Отходы монокристаллов рубина нашли применение в часовой промышленности. Многие монокристаллы применяются так же в качестве украшений (бриллиант, топаз, сапфир, рубин и др.). [c.38]
Арсенид галлия (njHpoKo применяемый полупроводник) имеет структуру типа сфалерита (см. рис.
 52, а). Об1.ясните строение GaAs, пользуясь методом валентных связей. [c.99]
52, а). Об1.ясните строение GaAs, пользуясь методом валентных связей. [c.99]Применение. Эти свойства, наряду с возможностью получения сложных форм без механической обработки, позволяют применить СУ в качестве специальных сосудов для производства полупроводниковых материалов, больших оптических монокристаллов, фторцирконатных и фторгафнатных стекол, имеющих малые оптические потери, полупроводникового арсенида галлия, металлов, в частности индия, и сплавов, деталей аппаратуры для особо агрессивных сред. [c.464]
Арсенид галлия GaAs и антимонид индия InSb получают сплавлением элементарных веществ. Это полупроводники, имеющие важное практическое значение. [c.277]
Неметаллическая природа азота и его аналогов выражена несколько слабее по сравнению с соседями из VI и VII групп периодической системы. Тем не менее и азот и его аналоги при повышенной температуре охотно взаимодействуют со многими металлами, образуя так называемые нитриды, фосфиды, арсениды и антимониды металлов, например [c. 79]
79]
С некоторыми металлами мышьяк образует соединения — арсениды, многие из которых можно рассматривать как продукты замещения водорода в арсине атомами металла — например. Сиз As, СазАзг. [c.447]
Неорганическая химия (1989) — [ c.49 ]
Неорганическая химия (1981) — [ c.335 ]
Химический энциклопедический словарь (1983) — [ c.56 ]
Руководство по неорганическому синтезу Т 1,2,3,4,5,6 (1985) — [ c.985 , c.1037 , c.1038 , c.1125 , c.1140 , c.1248 , c.1330 ]
Курс аналитической химии Том 1 Качественный анализ (1946) — [
c.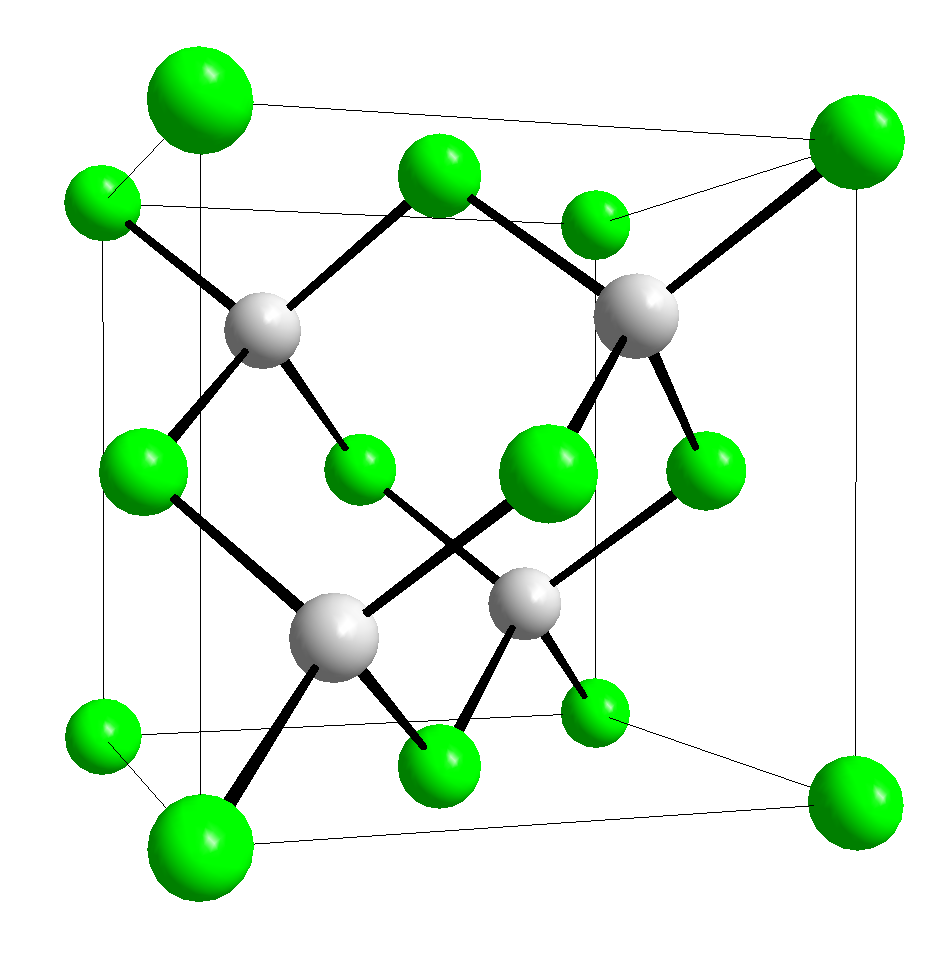 163
]
163
]
Химия Краткий словарь (2002) — [ c.36 ]
Большой энциклопедический словарь Химия изд.2 (1998) — [ c.56 ]
Химия справочное руководство (1975) — [ c.88 ]
Курс неорганической химии (1963) — [ c.712 ]
Неорганическая химия (1974) — [ c.266 ]
Неорганическая химия Издание 2 (1976) — [ c.314 ]
Общая химия 1982 (1982) — [ c.425 ]
Общая химия 1986 (1986) — [ c.411 ]
Общая и неорганическая химия (1981) — [ c.432 ]
Учебник общей химии 1963 (0) — [
c. 265
]
265
]
Неорганическая химия (1981) — [ c.335 ]
Неорганическая химия (1978) — [ c.343 ]
Общая химия Издание 4 (1965) — [ c.274 ]
Общая химия Издание 18 (1976) — [ c.421 ]
Общая химия Издание 22 (1982) — [ c.425 ]
Общая и неорганическая химия (1994) — [ c.426 ]
Неорганическая химия (1969) — [ c.398 ]
Общая и неорганическая химия (1981) — [ c.381 ]
Методы разложения в аналитической химии (1984) — [ c.0 ]
Стереохимия (1949) — [
c.300
,
c. 306
]
306
]
Основы общей химии Т 1 (1965) — [ c.452 , c.458 ]
Основы общей химии Том 3 (1970) — [ c.111 , c.136 ]
Курс неорганической химии (1972) — [ c.637 ]
Арсениды – Химический справочник
Арсенид германия — бинарное неорганическое соединениегермания и мышьяка с формулой GeAs. Арсенид германия Общие Систематическоенаименование
Арсенид самария — неорганическое соединениесамария и мышьяка с формулой SmAs, кристаллы. Арсенид самария Общие Систематическоенаименование
Арсенид марганца — неорганическое соединение металла марганца и мышьяка с формулой MnAs, тёмно-серые кристаллы, не
Арсенид лития — бинарное неорганическое соединениелития и мышьяка с формулой LiAs, кристаллы. Арсенид лития Общие
Арсенид лития Общие
Диарсенид рутения — бинарное неорганическое соединениерутения и мышьякас формулой RuAs2, кристаллы. Диарсенид рутения Общие Систематическоенаименование
Диарсенид палладия — бинарное неорганическое соединениепалладия и мышьякас формулой PdAs2, кристаллы, не растворяется в воде.
Диарсенид триртути — неорганическое соединениертути и мышьякас формулой Hg3As2, кристаллы. Диарсенид триртути Общие Систематическоенаименование Диарсенид
Полкановит — очень редко встречающийся минерал родия из класса арсенидов. Относится к типу «сернистые соединения
Скуттерудит — минерал, арсенид кобальта и никеля из группы скуттерудита. Общая теоретическая химическая формула минералов
Сперрилит — минерал, арсенид платины PtAs2, который является основной рудой платины. Был назван в честь
Был назван в честь
Арсенид галлия | CMK Ltd.
Компания CMK производит полуизолирующие и полупроводниковые пластины и слитки из арсенида галлия методом Чохральского с жидкостной герметизацией или методом вертикальной направленной кристаллизации. Требуемые электрические параметры достигаются благодаря использованию сырья чистотой 6N (галлия и мышьяка). Чтобы получить нужный уровень концентрации, применяются легирующие примеси: цинк, кремний и теллур.
Производство включает выращивание монокристаллического и поликристаллического арсенида галлия в тиглях из пиролитического нитрида бора и особо чистого кварца. Мы производим монокристаллические пластины и цельные слитки диаметром 2–4 дюйма, пригодные для эпитаксии и применения в высокочастотных и оптоэлектронных приборах.
Специально обученный квалифицированный персонал производит высококачественный материал с учетом всех пожеланий заказчика.
| Характеристики монокристаллического арсенида галлия |
| Полуизолирующий арсенид галлия,нелегированный | Полупроводниковый арсенид галлия, дырочная и электронная проводимость |
| Диаметр | пластины: 2–4 дюйма слитки и синтез: 2–6 дюймов |
| Толщина | пластины: 325–750 мкм слитки и синтез: 2–6 дюймов |
| Легирующая примесь | – | Цинк, кремний, теллур |
| Концентрация носителей | – | электронная проводимость 1 x 1016 – 2 x 1018 см-3 дырочная проводимость 1 x 1016 – 5 x 1019 см-3 |
| Ориентация кристалла | (100), (110), (111) |
| Разориентация | до 15°, более 15° при необходимости |
| Удельное сопротивление | >1 x 107 Ом•см | >1 x 10-3 Ом•см |
| Холловская подвижность | >6000 см2 В-1с-1 | электронная проводимость >1500 см2/В-1·с-1; дырочная проводимость: низкая |
| Плотность ямок травления (EPD) | 4 см-2 | метод Чохральского с жидкостной герметизацией: 4 см-2 метод вертикальной направленной кристаллизации: 3 см-2 |
| Обработка поверхности | пластины: резка / притир / травление / одностороннее и двустороннее полирование слитки и синтез: шлифование / выращивание / резка |
| Ориентация срезов | по стандарту SEMI или EJ |
| Упаковка | стандартная упаковка / EMPAK / Fluoroware / Fluoroware с герметизацией при помощи азота |
Кроме того, мы предоставляем поликристаллический арсенид галлия в виде плиток и слитков диаметром 0,5–4,25 дюйма. Наши продукты изготавливаются под высоким давлением из особо чистого сырья с точным стехиометрическим контролем. Чистота каждого слитка определяется с применением метода масс-спектрометрии тлеющего разряда.
Наши продукты изготавливаются под высоким давлением из особо чистого сырья с точным стехиометрическим контролем. Чистота каждого слитка определяется с применением метода масс-спектрометрии тлеющего разряда.
Поликристаллический арсенид галлия используется в качестве сырья для дальнейшей обработки и применения в различных сферах.
| Характеристики поликристаллического арсенида галлия |
| Полуизолирующий арсенид галлия,нелегированный | Полупроводниковый арсенид галлия, дырочная и электронная проводимость |
| Диаметр | пластины: 0,5–4,25 дюйма слитки и синтез: 2–6 дюймов |
| Толщина | пластины: 0,5–40 мм слитки и синтез: 50–100 мм |
| Легирующая примесь | – | Цинк, кремний, теллур |
| Концентрация носителей | – | электронная проводимость 1 x 1016 – 2 x 1018 см-3 дырочная проводимость 1 x 1016 – 5 x 1019 см-3 |
| Удельное сопротивление | >1 x 107 Ом•см | >1 x 10-3 Ом•см |
| Холловская подвижность | >1 x 103 см2 В-1с-1 | электронная проводимость >1500 см2 В-1 с-1 p-дырочная проводимость: низкая |
| Плотность травления (EPD) | 4 см-2 | метод Чохральского с жидкостной герметизацией: 4 см-2 метод вертикальной направленной кристаллизации: 3 см-2 |
| Обработка поверхности | пластины: резка / травление слитки и синтез: шлифование / выращивание / резка |
| Ориентация срезов | по стандарту SEMI или EJ |
| Упаковка | тандартная упаковка / Fluoroware / Fluoroware с герметизацией при помощи азота |
Упаковка изделий из арсенида галлия
Мы предоставляем различные виды упаковки нарезанных и шлифованных пластин:
- отдельные контейнеры Fluoroware;,
- лотки Fluoroware с раздельной герметизацией в инертной среде,
- кассеты Empak на 25 пластин,
- стандартная упаковка для цельных слитков и кристаллов;
Область применения арсенида галлия
Монокристаллический арсенид галлия
Полуизолирующий арсенид галлия
- диаметр: 2, 3 и 4 дюйма (плиты и слитки)
- без легирования кремнием
Полупроводниковый арсенид галлия
- диаметр: 2, 3 и 4 дюйма (плиты и слитки)
- электронная проводимость: легирование кремнием и теллуром
- дырочная проводимость: легирование цинком
Область применения: производство светодиодов, высокотехнологичных приборов, микроэлектромеханических систем, устройств с питанием от солнечной энергии, активных компонентов, интегральных микросхем, телекоммуникационных деталей и т. д.
д.
Поликристаллический арсенид галлия
Плиты из арсенида галлия
- диаметр: 0,5–4,25 дюйма
- толщина: 0,5–40 мм
- без легирования кремнием
- электронная проводимость: легирование кремнием и теллуром; дырочная проводимость: легирование цинком
Слитки из арсенида галлия диаметром до 6 дюймов для выращивания кристаллов методом вертикальной направленной кристаллизации
- диаметр: 4,5–6 дюймов
- толщина: 50–100 мм
- без легирования кремнием
- электронная проводимость: легирование кремнием и теллуром; дырочная проводимость: легирование цинком
- Метод выращивания: метод Чохральского с жидкостной герметизацией и метод вертикальной направленной кристаллизации
Область применения: применяется как исходный материал для производства других изделий из арсенида галлия (светодиодов, устройств волоконно-оптической связи, высокочастотных схем, высокопроизводительных фотогальванических приборов и т. д.)
Заготовки для оптических компонентов
Пластины из арсенида галлия для оптических компонентов
- диаметр: 0,5–4,25 дюйма
- толщина: 1–20 мм
- без легирования кремнием
- Метод выращивания: метод Чохральского с жидкостной герметизацией
Область применения:устройства беспроводной связи, псевдоморфные транзисторы с высокой подвижностью электронов, оптоэлектронные компоненты (фотодиоды, фототранзисторы, фоторезисторы, интегральные оптические схемы, оптосоединители, лазерные диоды, инфракрасные светодиоды), микросхемы, устройства волоконно-оптической связи, устройства с питанием от солнечной энергии и т. д.
Арсенид железа – особый класс сверхпроводников | Блоги
Физики из Национальной лаборатории Департамента энергетики США в г. Эймсе (Ames Labolatory) экспериментально продемонстрировали, что механизм сверхпроводимости в недавно открытых сверхпроводниках из арсенида железа является уникальным по отношению ко всем другим известным классам сверхпроводников. Это открытие совместно с потенциально хорошей способностью проводить ток благодаря низкой анизотропии может открыть дверь для многообещающих приложений в области передачи тока с нулевым сопротивлением.
Исследование, возглавляемое Русланом Прозоровым, показало, что образование электронных пар в арсениде железа весьма вероятно очень отличается от других типов известных сверхпроводников. В сверхпроводящих материалах ниже критической температуры электроны объединяются в пары, называемые куперовскими, и эти пары ведут себя идентично. Наиболее известная особенность сверхпроводников – прохождение электрического тока без сопротивления – обусловлена коллективным движением куперовских пар.
Однако сверхпроводники имеют еще одно присущее им свойство, которое отличает их от «хороших металлов», – они вытесняют слабое магнитное поле из своего объема (эффект Мейснера). В любом случае, слабое магнитное поле проникает только в узкую область поверхности сверхпроводника. Глубина этой области известна как лондоновская глубина проникновения.
«Изменение лондоновской глубины проникновения в зависимости от температуры определяется структурой энергетической щели, которая, в свою очередь, зависит от квантового механизма формирования электронных пар, – сказал Прозоров. – Лондоновская глубина проникновения является одной из основных экспериментально измеряемых величин при изучении сверхпроводников».
В обычных сверхпроводниках, включая свинец и ниобий, зависимость лондоновской глубины проникновения от температуры экспоненциальная при низких температурах. В высокотемпературных сверхпроводниках класса купраты, зависимость линейная, и в магнии дибориде зависимость также экспоненциальная, но требует двух разных энергетических щелей для объяснения данных во всем температурном диапазоне.
В противоположность этому, группа из Лаборатории Эймса обнаружила, что сверхпроводники из арсенида железа демонстрируют степенной – почти квадратичный – закон изменения глубины проникновения с температурой.
Так как лондоновская глубина проникновения связана с поведением электронных пар, полученные данные наводят на мысль, что поведение электронных пар в сверхпроводниках из арсенида железа также отлично от такового в других известных сверхпроводниках.
Вдобавок группа обнаружила, что полученные экспериментальные данные для сверхпроводников из арсенида железа могут быть объяснены только при предположении о наличии двух разных энергетических щелей. Таким образом эти сверхпроводники проявляют свойства как высокотемпературных сверхпроводников купратов, так и магния диборида.
Руслан Прозоров отметил, что уникальные свойства сверхпроводников из арсенида железа позволяют ему предполагать, что в этих материалах температура перехода в сверхпроводящее состояние может быть близка к комнатной.
Вы можете подписаться на нашу страницу в LinkedIn!
Арсениды – Энциклопедия по машиностроению XXL
Практически достоинством диода на основе арсенида галлия является то, что в широком диапазоне температур от 1 до по меньшей мере 400 К прямое падение напряжения на диоде при постоянном токе через диод зависит от температуры почти линейно. Так же ведут себя и кремниевые диоды при температурах выше 30 К, причем линейность у них даже лучше, чем [c.254]Полупроводниковый лазер генерирует когерентное излучение в результате процессов, происходящих в р-и-переходе на полупроводниковом материале. На рис. 3.8 показана схема полупроводникового лазера на арсениде галлия. Кристалл имеет размеры около 0,5…1,0 мм . Верхняя его часть 2 представляет собой полупроводник р-типа, нижняя / — п-типа, между ними имеется р-п-переход 4 толщиной около 0,1 мкм. [c.123]
При подаче напряжения на выводы р-п-переход генерирует излучение, длина волны которого для арсенида галлия составляет X) = 0,82 мкм и 2 = 0,9 мкм (инфракрасная область). Для других материалов длина волны излучения может лежать в широком диапазоне — от ультрафиолетовой до инфракрасной области. [c.124]
Эффект Ганна. В 1963 г. Дж. Ганн, изучая поведение арсенида галлия в области сильных полей, обнаружил новое явление, заключающееся в возникновении колебаний тока с частотой 10 — 256 [c.256]
Излучение, возникающее при переходах с верхних уровней на нижние, является спонтанным. В среде с инверсной населенностью это спонтанное излучение индуцирует дополнительные переходы. Для того чтобы создать квантовый генератор, в среде с инверсной населенностью необходимо обеспечить условия автоколебательного режима. Такой режим достигается за счет помещения активной среды, т. е. вещества, в котором создается инверсная населенность, -В резонатор, выполняющий роль положительной обратной связи. Резонатор обеспечивает также пространственную и временную когерентность излучения. Простейший резонатор представляет собой два плоскопараллельных зеркала, одно из которых является полупрозрачным. В рубиновом лазере резонатором служат отполированные торцы рубинового стержня, покрытые тонким слоем металла, в полупроводниковом инжекционном лазере на арсениде галлия— это тщательно полированные боковые грани, перпендикулярные плоскости р-и-перехода. [c.318]Первый полупроводниковый лазер был выполнен на арсениде галлия (ОаАз) Ходом в 1962 г. Этот лазер обладал очень большой вероятностью излучательной рекомбинации. Лазер на арсениде галлия (Я = 0,84 мкм) относится к так называемым инжекционным лазерам на р —п-переходе. Обычно плавные р-н-переходы создают путем диффузии акцепторных примесей (цинк, кадмий и др.) в материал, легированный донорными примесями (теллур, селен и др.). [c.297]
Отличительной чертой всех полупроводниковых лазерных материалов, в том числе и арсенида галлия, является очень высокий по сравнению с другими лазерными материалами (кристаллы, стекла, жидкости, газы) коэффициент усиления электромагнитного излучения. Благодаря этому удается выполнить условие генерации для миниатюрных полупроводниковых образцов. Типичный лазер на арсениде галлия показан на рис. 35.24, а. Для получения генерации две противоположные поверхности полупроводника полируют и делают плоскопараллельными, а две другие оставляют грубо обработанными, чтобы предотвратить генерацию в нежелательных направлениях. Обычно обе отражающие поверхности не имеют отражающих покрытий, так как показатель преломления полупроводника достаточно большой и от полированных торцов отражается примерно 35 % падающего излучения. Активная область представляет собой слой толщиной около 1 мкм, т. е. немного больше запирающего слоя (примерно 0,2 мкм). В свою очередь поперечные размеры лазерного пучка гораздо больше (около 40 мкм) толщины активной области (рис. 35.24, б). Следовательно, лазерный пучок занимает довольно большое пространство в р- и п-областях. Однако поскольку поперечные размеры пучка все же относительно невелики, выходное излучение имеет большую расходимость (несколько градусов). [c.297]
Кроме лазера на арсениде галлия, применяются и другие типы полупроводниковых лазеров. Крупные успехи в разработке полупроводниковых лазеров связаны с появлением инжекционных лазеров на гетеропереходах. Так называют сложные р —п-структуры, состоящие из полупроводниковых материалов с различной шириной запрещенной зоны. [c.297]
Полупроводниковые ТС используют обычно для измерения температур ниже О °С [11, 43, 47]. Основное преимущество полупроводниковых ТС состоит в том, что их чувствительность гораздо выше чувствительности металлических ТС при низких температурах. В низкотемпературной термометрии применяют германиевые [11, 35, 40—42], угольные [44], арсенид-галлиевые ТС [45]. [c.179]
Галия арсенид + Меди хлорид + [c.884]
Индия арсенид Свинца ниобат 1 =b [c.884]
Изложено термодинамическое обоснование возможности ретроградного распада с выделением жидкой фазы. Приведены оригинальные данные о прецизионном построении кривых ретроградного солидуса в важнейших полупроводниковых системах с участием германия, кремния, арсенида индия и др. Рассмотрены кинетика распада и структурный механизм этого процесса. Обосновано использование диаграммы фазовых равновесий при выборе уровня легирования полупроводников и режимов их термической обработки. Описаны возможности направленного изменения свойств материалов, обеспечивающих надежную работу электронных устройств. [c.51]
Сходным образом небольшие количества оксида мышьяка ускоряют коррозию стали в кислотах (например, в HjSO ), возможно, благодаря формированию арсенидов. А будучи добавленным в больших количествах (jw 0,05 % в 72 % HjSOJ, оксид мышьяка становится эффективным ингибитором коррозии, вероятно, вследствие того, что элементарный мышьяк, имеющий высокое водородное перенапряжение, осаждается на катодных участках. Соли олова имеют аналогичный ингибирующий эффект и используются для защиты стали от разрушения травильными кислотами при удалении окалины. — Примеч. авт. [c.58]
Для улучшения условий работы полупроводникового лазера и обеспечения непрерывного режима генерации кристалл необходимо охлаждать до низких температур. Мощность лазера на арсениде галлия при температуре жидкого азота в импульснопериодическом режиме составляет 100 Вт, в непрерывном режиме — 10 Вт. Лучшие образцы полупроводниковых лазеров могут работать при нормальных температурах. [c.124]
Многие полупроводники, в частности арсеаид галлия, имеют достаточно сложную зонную структуру. Так, зона проводимости арсенида галлия кроме минимума E k) при k=0 имеет втор ой минимум в направлении [100] при 0,8 о, где, о — волновой [c.257]
Оптические свойства. Исследование оптических свойств кристаллических полупроводников дает обширную информацию об их зонной структуре. Данные об энергетическом спектре аморфных полупроводников также могут быть получены из оптических измерений. Первостепенная роль отводится при этом измерениям спектров поглощения. Спектры поглощения аморфных полупроводников удобно сравнить со спектром тех же материалов в кристаллическом состоянии. Это можно сделать в случаях германия, кремния, соединений селена и теллура. На рис. 11.14 в качестве примера приведен край спектра оптического поглощения аморфного кремния, который сравнивается с соответствующим спектром кристаллического кремния. Аналогичные данные получены для аморфного германия, арсенида и антимонида индия и некоторых других полупроводников. [c.367]
Среди неэ( ективных фотоэмиттеров мы привели, в частности, арсенид галлия (GaAs). Однако этот фотоэмиттер (сильнолегированный /j-полупроводник) можно сделать эффективным, если нанести на его поверхность тонкую пленку [c.173]
На рис. 7.14 схемати- р чески изображен солнечный п -элемент, включенный в электрическую цепь. Большое практическое примене- ние находят солнечные элементы на основе кремния (точнее говоря, па основе контакта p-Si и w-Si) КПД этих элементов достигает 15 %. Применяются также элементы на основе арсенида галлия (GaAs). Имея несколько более низкий КПД, они в то же время характеризуются большей стойкостью к радиационным повреждениям. [c.181]
Арсенид галлия среди соединений А ” В занимает особое положение. Большая ширина запрещенной зоны (1,4 эВ), высокая подвижность электронов [0,85 м /(В-с)] позволяют создавать на его основе приборы, работающие при высоких температурах и высоких частотах. Первым полупроводником являлся GaAs, на котором в 1962 г. был создан инжекционный лазер. Он используется для изготовления светодиодов, туннельных диодов, диодов Ганна, транзисторов, солнечных батарей и других приборов. Для изготовления детекторов в инфракрасной области спектра, датчиков Холла, термоэлектрических генераторов, тензометров применяется анти-монид индия, имеющий очень малую ширину запрещенной зоны [c.291]
Арсенид – Arsenide – xcv.wiki
В химии арсенид – это соединение мышьяка с менее электроотрицательным элементом или элементами. Многие металлы образуют бинарные соединения, содержащие мышьяк, и их называют арсенидами. Они существуют со многими стехиометриями , и в этом отношении арсениды подобны фосфидам .
Арсениды щелочных металлов и щелочноземельных металлов
Группа 1 щелочные металлы и группа 2, щелочно – земельных металлов , образуют арсениды с изолированными атомами мышьяка. Они образуются при нагревании порошка мышьяка с избытком натрия с образованием арсенида натрия (Na 3 As). Структура Na 3 As сложна с необычно короткими расстояниями Na – Na 328–330 пм, которые короче, чем у металлического натрия. Это короткое расстояние указывает на сложную связь в этих простых фазах, т.е. они не являются, например, просто солями аниона As 3– . Соединение LiAs имеет металлический блеск и электрическую проводимость, указывающую на наличие металлических связей. Эти соединения представляют в основном академический интерес. Например, «арсенид натрия» является структурным мотивом, принятым во многих соединениях со стехиометрией A 3 B.
Обладая солевыми свойствами, гидролиз арсенидов щелочных металлов дает арсин :
- Na 3 As + 3 H 2 O → AsH 3 + 3 NaOH
Соединения III – V
Многие арсениды элементов группы 13 (группа III) являются ценными полупроводниками. Арсенид галлия (GaAs) имеет изолированные центры мышьяка со структурой цинковой обманки (структура вюрцита в конечном итоге также может образовываться в наноструктурах) и с преимущественно ковалентной связью – это полупроводник AIIIBV.
II – V соединения
Обращают на себя внимание арсениды элементов группы 12 (группа II). Было показано, что арсенид кадмия (Cd 3 As 2 ) представляет собой трехмерный (3D) топологический полуметалл Дирака, аналогичный графену . Cd 3 As 2 , Zn 3 As 2 и другие соединения четвертичной системы Zn-Cd-P-As имеют очень похожие кристаллические структуры, которые можно рассматривать как искаженные смеси кристаллических структур цинковой обманки и антифторита .
Полиарсениды
Арсениды переходных металлов
Анионики мышьяка, как известно, образуют катетеры, то есть образуют цепи, кольца и клетки. Минеральный скуттерудит ( CoAs 3 ) имеет кольца, которые обычно обозначаются как As 4-
4 . Назначить формальную степень окисления сложно, потому что эти материалы очень ковалентны и часто лучше всего описываются с помощью теории зон . Сперрилит (СПТ 2 ), как правило , описывается как Pt 4+
В качестве 4-
2 . Арсениды переходных металлов представляют интерес главным образом потому, что они загрязняют сульфидные руды, представляющие коммерческий интерес. Добыча металлов – никеля, железа, кобальта, меди – влечет за собой химические процессы, такие как плавка, которые представляют опасность для окружающей среды. В минерале мышьяк неподвижен и не представляет опасности для окружающей среды. Выделяемый из минерала мышьяк ядовит и подвижен.
Фазы Zintl
Структура субъединицы [As 7 ] 3– в фазе Zintl Cs 2 NaAs 7 .При частичном восстановлении мышьяка щелочными металлами (и родственными электроположительными элементами) образуются полиомышьяковые соединения, которые входят в фазы Цинтля .
Смотрите также
Рекомендации
<img src=”//en.wikipedia.org/wiki/Special:CentralAutoLogin/start?type=1×1″ alt=”” title=””>Арсенидов – обзор | ScienceDirect Topics
1.16.1.1 Синтез арсина
Arsine AsH 3 , обычно производится с помощью NaBH 4 восстановления AsCl 3 или As 2 O 3 , 16 или гидролизом арсениды щелочных металлов. 17 Небольшие количества очень чистого AsH 3 можно получить путем нагревания As 2 O 3 с LiAlH 4 , хотя общий выход низкий. 18 Потребность в сверхчистом AsH 3 для процессов CVD в электронной промышленности и его очень высокая токсичность привели к появлению множества патентов, касающихся синтеза и очистки арсина на месте. Было предложено хранение AsH 3 как [(C 6 F 5 ) 3 BAsH 3 ], из которого он выделяется при слабом нагревании. 19 Первичный (AsRH 2 ) и вторичный (AsR 2 H) арсины редко использовались в качестве лигандов, но их можно получить восстановлением соответствующих галогенарсинов, например.г., получение Me 3 SiCH 2 AsH 2 и (Me 3 SiCH 2 ) 2 AsH, 20 мышьяковой или мышиновой кислот, например AsMe 2 H, 21 и AsBuH 2 , 22 или гидролизом органических арсенидов металлов, например, AsPh 2 H. 23 AsRH 2 (R = 2, 6-диизопропилфенил, 2,4,6-триизопропилфенил) синтезированы и подробно охарактеризованы. 24
Было получено значительное количество триорганоарсинов, 7,12,13,15,25,26 , хотя в качестве лигандов было использовано гораздо меньшее количество. Традиционные способы включают реакцию AsX 3 или AsR 3- n X n ( n = 1 или 2) с RMgX или RLi в растворе эфира. Урожайность варьируется от плохой до хорошей в зависимости от группы R. Распространенные AsR 3 , изготовленные по этому маршруту: AsMe 3 , 27 AsEt 3 , 28,29 As n Pr 3 , 29 As (cyclo -C 6 H 11 ) 3 , 29 As (cyclo-C 5 H 9 ) 3 , 30 As (SiMe 3 ) 3 31 и As т Bu 3 . 31 Органоарсениды щелочных металлов Li (Na) AsR 2 могут реагировать с R’X с образованием AsR 2 R ‘. 32
Другие металлоорганические реагенты использовались реже, например, синтез As (CF 3 ) 3 из Hg (CF 3 ) 2 , 33 или AsMe 2 (SMe), полученный из AsMe 2 Cl и Pb (SMe) 2 . 34 Совсем недавно использовались реагенты AlR 3 , которые, как утверждается, дают высокие выходы и при соответствующих условиях более чистые продукты, чем пути Гриньяра или RLi.Таким образом, AlMe 3 и As 2 O 3 в Bu 2 O-диглиме дает высокий выход AsMe 3 , который отгоняют из реакционной смеси. 35 Широкий диапазон AsR 3 (R = Et, n Pr, i Pr, n Bu, i Bu, t Bu, CH 2 CH, MeCHCH , Me 3 SiCH 2 , Ph, Bz, мезитил) может быть получен с высокой чистотой из AlR 3 и хлордиоксарсолана, OCh3Ch3OAOsCl (сам получен из AsCl 3 и 1,2-этандиола). 26 Нагревание AlR 3 или RMgX с As (NMe 2 ) 3 дало хорошие выходы AsR 3 (R = Et, n Pr, n Bu, CH 2 CH), но маршрут не работает со стерически затрудненными R-группами. 36 Маршрут может быть успешно расширен до синтеза AsMe 2 R с использованием AsMe 2 NMe 2 . 37 Было собрано большое количество образцов 1 H и 13 C ЯМР третичных арсинов. 26,36,37 Триалкил- и смешанные арилалкиларсины обычно являются чувствительными к воздуху, высокотоксичными жидкостями с отталкивающими запахами. Триариларсины – твердые вещества, устойчивые на воздухе. Синтез и разделение хиральных арсинов подробно рассмотрен Уайлдом. 38
Третичные арсины обычно получают из соответствующего дигалогенорганического соединения и Li (Na \ K) AsR 2 в жидком аммиаке или т. Н. Наиболее распространенные примеры, сделанные по этому маршруту: Ph 2 As (CH 2 ) n AsPh 2 ( n = 1-3), Me 2 As (CH 2 ) 3 AsMe 2 , cis -R 2 AsCHCHAsR 2 (R = Me или Ph), o -C 6 H 4 (AsMe 2 ) 2 2 2 6,7,21,32 Тот же самый маршрут дает Ph 2 AsCH 2 AsPh 2 , 39 и Me 2 AsCH 2 AsMe 2 . 40 Реакция NaAsMe 2 с BrCH 2 CH 2 Br дает Me 2 AsAsMe 2 и CH 2 CH 2 , но очень низкий выход Me 2 AsCH 2 CH 2 AsMe 2 можно получить из NaAsMe 2 и ClCH 2 CH 2 Cl в жидком аммиаке при −78 ° C, и была описана по крайней мере одна серия комплексов . 41,42 Использование NaAsMePh и o -C 6 H 4 Cl 2 дает o -C 6 H 4 (AsMePh) 2 , из которых R * Разделяли диастереоизомеры R * и R *, S *. 43,44 Модель o -C 6 F 4 (AsMe 2 ) 2 выполнена как на схеме 1 и представляет собой аналог o -C 6 H 4 (AsMe 2 ) 2 с идентичными стерическими свойствами, но пониженной донорной силой. 45
Схема 1.
Как указано во введении, полидентатные арсиновые лиганды известны с 1960-х годов, и известно множество триподальных и факультативных три- и тетраарсинов. 6,7 Их синтез обычно происходит через вариации маршрутов, используемых для дневников. Недавно опубликованные примеры включают ClCH 2 C (CH 2 AsMe 2 ) 3 , полученный из NaAsMe 2 и C (CH 2 Cl) 4 (четвертый хлор не замещается), 46 и PhAs ( o -C 6 H 4 AsMe 2 ) 2 , приготовленные из PhAsCl 2 , n BuLi и o -BrC 6 H 6 H 4 AsMe 2 . 47 Взаимодействие MeC (CH 2 Cl) 3 с o -C 6 H 4 (AsMe 2 ) (AsMeNa) в thf дает тетраретичный и шестнадцатеричный арсин. ( I и II ), которые были разделены через их комплексы Co III . 48 Идентифицированы диастереоизомеры тетрадентатного арсина.
Би- и полидентатные лиганды, содержащие мышьяк в комбинации с другими донорами групп 15 или 16, также известны в течение многих лет. 6,7 Некоторые новые примеры показаны на рисунке 1.
Рисунок 1. Некоторые гибридные лиганды, содержащие доноры мышьяка (числа под структурами являются литературными ссылками на синтезы).
R 2 AsCH 2 CH 2 PR ′ 2 (R = t Bu, Cy, R ′ = Ph, i Pr) были приготовлены из циклического сульфата O 2 O2SOCh3Ch3O⎴, обработанные последовательно подходящими арсенидом и фосфидом лития, причем ключ состоит в том, чтобы сначала добавить более сильный нуклеофил, в противном случае получаются смеси. 59 Новые, чрезвычайно чувствительные к воздуху арсино (фосфино) метаны R 2 PCH 2 AsR ′ 2 (R = i Pr, R ′ = i Pr, т Bu, Cy; R, R ′ = Cy) с хорошим выходом получаются реакцией R 2 PCH 2 SnR ′ 3 с RLi, Me 2 NCH 2 CH 2 NMe 2 , и R ‘ 2 AsCl. 60
Арсенид – обзор | Темы ScienceDirect
1.2 Возникновение и причины появления мышьяка в подземных водах
Мышьяк может встречаться в естественных условиях примерно в 200 минералах в различной степени в виде элементарного мышьяка, мышьяка, сульфидов, оксидов, арсенита и арсенатов. Однако самые высокие концентрации мышьяка связаны с сульфидными минералами и оксидами металлов, особенно оксидами железа. Проблема загрязнения мышьяком может привести к появлению мест массового распространения этих минералов только в том случае, если геохимические условия способствуют высвобождению мышьяка из этих минералов.Геохимические условия, которые широко считаются причинами загрязнения подземных вод, – это pH, аэробная или восстанавливающая среда, поток подземных вод и транспорт. Самым распространенным минералом мышьяковой руды является пирит (FeS 2 ), за ним следуют халькопирит, галенит и марказит, где концентрации мышьяка могут достигать 10 мас.%. Помимо того, что пирит является важным рудным компонентом, он также может образовываться в осадочных средах в восстановительных условиях.
В аэробных условиях пирит может окисляться до оксидов железа с выделением сульфата, кислотности и мышьяка вместе с микроэлементами.Реакции окисления пирита протекают по уравнению
FeS2 + 15 / 4O2 + 7 / 2h3O → FeOh4 + 2SO4−2 + 4H +
Таким образом, деятельность человека вокруг добычи угля часто является причиной проблем с мышьяком в угольных шахтах. К счастью, в большинстве случаев мобилизация мышьяка в грунтовые и поверхностные воды низкая из-за высокого удержания мышьяка в связанных минералах. Мышьяк также может выделяться из арсенопирита (FeSA) в аэробных условиях, и во многих водоносных горизонтах по всему миру понижение уровня грунтовых вод считается причиной создания аэробной среды за счет поступления кислорода из атмосферы [29,30].Другая школа мысли [31,32] заключается в том, что выщелачивание мышьяка, вызванное биопосредованным восстановительным растворением оксигидроксидов железа, содержащих мышьяк, в основном является причиной проблемы загрязнения мышьяком в бассейне дельты Бенгалии. Для уменьшения содержания оксигидроксидов в аллювиальных водоносных горизонтах требуется органическое вещество (ОВ), источник которого может быть антропогенным (плохие санитарные условия, поверхностные почвы) или аутигенным. Хотя органическое вещество способствует сокращению выбросов, поверхностный источник такого органического вещества почти исключен [33], в отличие от некоторых наблюдений [14] в случае загрязненных мышьяком грунтовых вод в пакистанском Муззафаргархе.В бассейне дельты Бенгалии богатые органическими веществами флювиодельтовые отложения, которые были отложены во время высокого уровня древостоя в середине голоцена [34], оказались связаны с серьезной проблемой загрязнения мышьяком.
Аутогенные сульфидные минералы, содержащие мышьяк, могут образовываться в сильно восстановительных условиях в озерах, океанах и водоносных горизонтах. Условия окисления, которые часто вызывают растворение мышьяка из сульфидных минералов, могут возникать в неглубоких водоносных горизонтах, а не в глубоких водоносных горизонтах. Однако грунтовые воды могут оставаться в кислородных условиях в течение 5000 лет, когда сами связанные с ними отложения бедны органическими веществами, как в водоносном горизонте песчаника Шервуд в Соединенном Королевстве [35].В районе Тераи в Непале источник мышьяка считается геогенным [36], где загрязнение подземных вод мышьяком связано с восстановительным растворением оксигидроксида феррооксида.
В регулировании окислительно-восстановительных условий восстанавливающих водоносных горизонтов роль органического вещества широко высказывалась [37], хотя до сих пор остаются некоторые споры о природе органического вещества. Быстрое захоронение органического вещества вместе с отложениями способствует микробной деятельности, которая создает восстановительные условия, благоприятные для образования сульфидных минералов, содержащих мышьяк [32–37].Сточные воды, отходы животноводства и жизнедеятельности человека (антропогенное органическое вещество) также вызывают восстановление водного оксида железа и высвобождение сорбированного мышьяка в неглубокие подземные водоносные горизонты (<30 м), хотя поверхностный источник органического вещества в запуске такого процесса восстановления считается крайне маловероятным [ 14]. Однако ухудшение условий в глубоких (> 30 м) водоносных горизонтах, по-видимому, связано с естественным органическим веществом. В различных частях Азии наступление восстановительных условий в отложениях и последующие условия окисления в водоносных горизонтах в значительной степени были признаны ответственными за проблему загрязнения подземных вод мышьяком.После высвобождения мышьяка из кристаллической решетки и его растворения в воде накопление мышьяка в водоносном горизонте может продолжаться, если только его не вымывают за счет перемещения грунтовых вод с течением времени. Медленное движение грунтовых вод (из-за низкой скорости пополнения) является причиной многих водоносных горизонтов с высоким содержанием мышьяка в странах Юго-Восточной Азии. Таким образом, низкие концентрации мышьяка в глубоких и прибрежных водоносных горизонтах в Бангладеш и других местах объясняются интенсивным движением грунтовых вод и высокой скоростью их пополнения.
В некоторых геологически молодых и плохо промытых засушливых и полузасушливых регионах мира, таких как внутренние бассейны Аргентины и юго-запада США, условия высокого pH привели к десорбции мышьяка с минеральных поверхностей [38].Минеральное выветривание и сильное испарение приводят к условиям высокого pH. Хорошо известно, что при аэробном режиме и режиме pH от низкого до нейтрального адсорбция мышьяка, особенно As (V) на оксидах железа, очень сильная, концентрация в воде низкая, а десорбция мышьяка благоприятна при высоком pH. Также наблюдалась роль микробов в уменьшении и мобилизации мышьяка [39,40].
На концентрацию мышьяка в природной среде влияют многие факторы, такие как органические и неорганические компоненты почвы, статус окислительно-восстановительного потенциала.Вулканическая деятельность и эрозия горных пород и минералов также являются источниками выброса мышьяка в окружающую среду, равно как и антропогенная деятельность. Вещества, содержащие мышьяк, такие как консерванты для древесины, краски, лекарства, красители, металлы и полупроводники, также могут выделять мышьяк непосредственно в окружающую среду. Применение в сельском хозяйстве (пестициды, удобрения), горнодобывающая промышленность, плавка, захоронение земель и другие виды промышленной деятельности способствуют загрязнению окружающей среды мышьяком. Присутствие мышьяка в воде связано с природной и антропогенной деятельностью.
Вода – одно из основных средств переноса мышьяка в окружающей среде. В морской воде мышьяк встречается в пятивалентной, трехвалентной и метилированной формах. Морская вода обычно содержит от 1,5 до 5 мкг / л мышьяка [41]. В фотической зоне морской воды было обнаружено высокое содержание трехвалентной формы из-за того, что пятивалентный мышьяк превращается в трехвалентный мышьяк и органо-мышьяковые соединения в результате биологической активности. В естественных условиях мышьяк преобладает в местах с высокой геотермальной активностью в водной среде.Во втором регионе Чили водотоки характеризуются высоким содержанием мышьяка (100–1000 мг / л), что в основном связано с геотермальной активностью и четвертичным вулканизмом в Андах Кордильеры [20]. Промышленная деятельность также вызывает серьезные проблемы с загрязнением близлежащих подземных вод. Подземные воды в Реппеле (северная Бельгия), промышленной зоне, загрязненной мышьяком и тяжелыми металлами, содержат до 31 000 мг / л [42].
Микробные агенты могут влиять на степень окисления мышьяка в воде и могут опосредовать метилирование неорганического мышьяка с образованием органических соединений мышьяка [43].Микроорганизмы могут окислять арсенит до арсената и восстанавливать арсенат до арсенита или даже до арсина (ASH 3 ). Бактерии и грибы могут восстанавливать арсенат до летучих метиларсинов. Морские водоросли превращают арсенат в нелетучие метилированные соединения мышьяка, такие как метил-мышьяковую кислоту (CH 3 AsO (OH) 2 ) и диметиларсиновую кислоту ((CH 3 ) 2 AsO (OH)) в морской воде. Пресноводные, морские водоросли и водные растения синтезируют сложные жирорастворимые соединения мышьяка [44].Сообщалось, что органические соединения мышьяка обнаруживаются в поверхностных водах чаще, чем в грунтовых. По сообщениям, пробы поверхностных вод содержат низкие, но обнаруживаемые концентрации мышьяка, включая метил мышьяковую кислоту и диметиларсиновую кислоту. Сообщается, что метил-мышьяк составляет до 59% от общего количества мышьяка в озерной воде. Сообщается, что в некоторых озерах доминирующим видом является диметиларсиновая кислота, и ее концентрации, по-видимому, меняются в зависимости от сезона в результате биологической активности в воде.На рис. 1.5 показаны пути распространения мышьяка в окружающей среде.
Рисунок 1.5. Цикл мышьяка в окружающей среде.
(Адаптировано из [45]).Мышьяк был обнаружен в более высоких концентрациях в подземных источниках питьевой воды, чем в поверхностных водах. Концентрации мышьяка в окружающей среде представлены в таблице 1.2.
Таблица 1.2. Концентрации мышьяка в окружающей среде (Агентство по охране окружающей среды США 2000)
| Окружающая среда | Диапазон концентраций мышьяка | ||
|---|---|---|---|
| Воздух, нг / м3 | 1.5–53 | ||
| Дождь из незагрязненного океанического воздуха, мкг / л (ppb) | 0,019 | ||
| Дождь из земного воздуха, мкг / л | 0,46 | ||
| Реки, мкг / л | 906 264|||
| Озера, мкг / л | 0,38 – л, 000 | ||
| Грунтовая (колодезная) вода, мкг / л | & lt; 1.0 и & gt; л, 000 | ||
| Морская вода, мкг / л | 0,15–6,0 | ||
| Почва, мг / кг (ppm) | 0.л – 1000 | ||
| Отложения ручья / реки, мг / кг | 5,0–4000 | ||
| Осадки озера, мг / кг | 2,0–300 | ||
| Магматические породы, мг / кг | 0,3 – l13 | ||
| Метаморфическая порода, мг / кг | 0,0–143 | ||
| Осадочная порода, мг / кг | 0,1–490 | ||
| Биота: зеленые водоросли, мг / кг | 0,5–5,0 90 | Биота: бурые водоросли, мг / кг | 30 |
Арсениды | AMERICAN ELEMENTS ®
Наблюдение двумерной проводимости в ультратонких полевых транзисторах на основе арсенида германия., Грилло, Алессандро, Ди Бартоломео Антонио, Урбан Франческа, Пассакантандо Маурицио, Каридад Хосе М., Сан Джианбо и Камилли Лука , ACS Appl Mater Interfaces, 09 марта 2020 г., (2020)
Кристаллическая структура и химический состав тетраарсенида трикадмия дигермания, CdGeAs., Томпсон, Майкл Р., Райли Брайан Дж., Боуден Марк Э., Ольшта Мэтью Дж., Эдвардс Дэнни Дж., Крам Джаррод В., Джонсон Брэдли Р. и Чонг Сэхва , Acta Crystallogr E Crystallogr Commun, 2019 сен 01, том 75, выпуск Pt 9, p.1291-1296, (2019)
Модулированная теплопроводность двумерного гексагонального арсенида бора: инженерное исследование деформации., Раиси, Мостафа, Ахмади Сомайех и Раджабпур Али , Nanoscale, 21 ноября 2019 г., Volume 11, Issue 45, p.21799-21810, (2019)
Полиарсениды самария, полученные из наномасштабного мышьяка., Schoo, Christoph, Bestgen Sebastian, Egeberg Alexander, Seibert Jasmin, Konchenko Сергей Н., Фельдманн Клаус и Роски Петер В. , Angew Chem Int Ed Engl, 22 марта 2019 г., том 58, выпуск 13, стр. 4386-4389, (2019)
Исследование бактерицидного действия лазера на арсениде галлия и алюминия на анаэробные фотосенсибилизированные пародонтопатии., Додани, Киран, Кхаре Неха, Батини Чандрахас, Мишра Суприя, Инамдар Мохаммед Нк и Наша Амит , J Contemp Dent Pract, 2019 Mar 01, Volume 20, Issue 3, p.385-389, (2019)
Фотоэлектрический эффект ускоряет процессы электрохимической коррозии и наноимпринта на пластинах арсенида галлия., Guo, Chengxin, Zhang Lin, Sartin Matthew М., Хань Ляньхуань, Тянь Чжао-У, Тянь Чжун-Цюнь и Чжань Дунпин , Chem Sci, 21 июня 2019 г., том 10, выпуск 23, стр.5893-5897, (2019)
Солнечные элементы из арсенида галлия, выращенные с помощью гидридной парофазной эпитаксии со скоростью, превышающей 300 мкм / ч., Metaferia, Wondwosen, Schulte Кевин Л., Саймон Джон, Джонстон Стив и Птак Аарон Дж. , Nat Commun, 2019 Jul 26, Volume 10, Issue 1, p.3361, (2019)
Эпитаксиально выращенные нанопровода III-арсенид-антимонид для оптоэлектронных приложений., Ren, Dingding, Ahtapodov Lyubomir, van Helvoort Antonius TJ, Weman Helge , и Fimland Bjørn-Ove , Нанотехнологии, 19 июля 2019 г., том 30, выпуск 29, стр.294001, (2019)
Настраиваемые запрещенные зоны 2D-арсенида галлия и графена в гетероструктуре графен / GaAs: исследование ab initio., Гонсалес-Гарсия, А., Лопес-Перес В., Гонсалес-Эрнандес Р., Родригес Дж. А., Милошевич М. В. и Петерс Ф. М. , J Phys Condens Matter, 2019 Jul 03, Volume 31, Issue 26, p.265502, (2019)
Оптимизация роста и характеристика регулярных массивов GaAs / AlGaAs нанопроволок ядро / оболочка для тандемных солнечных элементов на кремнии., Vettori, M, Piazza V, Cattoni A, Scaccabarozzi A, Patriarche G, Regreny P, Chauvin N, Botella C, Grenet G, Penuelas J и др. , Нанотехнологии, 22 фев 2019, Том 30, Выпуск 8, с.084005, (2019)
Двумерный гидрогенизированный изогнутый арсенид галлия: исследование ab initio., González-García, A, López-Pérez W, González-Hernández R, Rivera-Julio J, Espejo C, Milośević M V., и Петерс Ф. М. , J Phys Condens Matter, 11 декабря 2019 г., том 32, выпуск 14, стр.145502, (2019)
Сверхпроводящие гибридные нанопровода ванадий / арсенид индия., Бьергфельт, Мартин, Каррад Деймон Джеймс, Канне Томас, Агесен Мартин, Фьордалисо Элизабетта, Джонсон Эрик, Шоджаи Борзойе, Палмстрём Крис Дж., Крогструп Питер, Т. Джесперсен Санд и др. , Нанотехнологии, 4 апреля 2019 г. (2019 г.)
Произошла ошибка при настройке пользовательского файла cookie
Этот сайт использует файлы cookie для повышения производительности. Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка вашего браузера для приема файлов cookie
Существует множество причин, по которым cookie не может быть установлен правильно. Ниже приведены наиболее частые причины:
- В вашем браузере отключены файлы cookie.Вам необходимо сбросить настройки своего браузера, чтобы он принимал файлы cookie, или чтобы спросить вас, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает вас, хотите ли вы принимать файлы cookie, и вы отказались. Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файлы cookie.
- Ваш браузер не поддерживает файлы cookie. Если вы подозреваете это, попробуйте другой браузер.
- Дата на вашем компьютере в прошлом. Если часы вашего компьютера показывают дату до 1 января 1970 г., браузер автоматически забудет файл cookie.Чтобы исправить это, установите правильное время и дату на своем компьютере.
- Вы установили приложение, которое отслеживает или блокирует установку файлов cookie. Вы должны отключить приложение при входе в систему или проконсультироваться с вашим системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу. Чтобы предоставить доступ без файлов cookie потребует, чтобы сайт создавал новый сеанс для каждой посещаемой страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в cookie; никакая другая информация не фиксируется.
Как правило, в файлах cookie может храниться только информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта. Например, сайт не может определить ваше имя электронной почты, пока вы не введете его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступа к остальной части вашего компьютера, и только сайт, который создал файл cookie, может его прочитать.
Индивидуальные арсениды и арсенидные соединения
Продукты
ПОДРОБНЕЕ О НАШЕМ ПРЕДЛОЖЕНИИ В ОБЛАСТИ НЕОРГАНИЧЕСКОЙ ХИМИИ
Загрузите наш Каталог неорганических химикатов. Это 36-страничное руководство включает всесторонний обзор наших передовых химических возможностей, рассматривает проблемы и творческие решения для некоторых из наших основных неорганических химикатов, список производимых нами соединений и многое другое.
Если у вас есть вопросы или вам требуется индивидуальное решение для вашего приложения, свяжитесь с одним из наших химиков сегодня.
Materion позволяет нам производить широкий спектр материалов. Наши процессы будут различаться в зависимости от продукта, области применения и конечного использования, поэтому мы можем создавать соединения арсенида в точном соответствии с требованиями заказчика.
ПРИМЕНЕНИЕ АРСЕНИДНЫХ СОЕДИНЕНИЙ В НЕСКОЛЬКИХ ТЕХНИЧЕСКИХ ПРИМЕНЕНИЯХ
Арсениды традиционно используются в различных промышленных и потребительских целях.Некоторые из распространенных применений включают:
- Полупроводники и электронные устройства
- Оптоэлектронные устройства, такие как светодиоды
- Солнечные элементы
- Пестициды и инсектициды
- Упрочнение сплавов Cu и Pb
РАЗНООБРАЗНЫЕ ФОРМЫ И МАТЕРИАЛЫ АРСЕНИДА
Наши высококачественные соединения арсенида доступны в нескольких формах, включая кусочки, комки и порошки, в зависимости от ваших потребностей. Они доступны в следующих стандартных и нестандартных составах:
АсБр 3 | AsCl 3 | Asl 3 | As 2 O 3 |
As 2 O 5 | As 2 Se 3 | As 2 Te 3 | …и более |
Найдите в нашем онлайн-каталоге неорганических химикатов арсенид и другие химические составы.
ПРЕИМУЩЕСТВА ЭКСПЕРТИЗЫ ХИМИЧЕСКОЙ ПЕРЕРАБОТКИ МАТЕРИАЛА
Наш более чем 50-летний опыт производства неорганических химикатов позволяет нам правильно обрабатывать и обрабатывать тысячи химикатов к удовлетворению потребностей наших клиентов. Наша талантливая команда химиков позволяет нам:
- Работа с экологически чувствительными и химически активными материалами
- Предлагаем индукционную плавку, вакуумную и инертную обработку
- Адаптировать материалы к точным спецификациям
- Разработка новых экспериментальных материалов с заданными физическими свойствами
- Масштабирование объемов производства от НИОКР до полного уровня производства
Проконсультируйтесь с химиком Materion, чтобы обсудить ваш продукт и выбрать лучшее соединение арсенида, соответствующее вашим требованиям.Заинтересованы в информации о ценах? Используйте нашу форму запроса предложения, чтобы предоставить подробную информацию о ваших требованиях к соединениям арсенида.
границ | Флюсовый рост кристаллов фосфидов и арсенидов
Введение
Фундаментальные исследовательские цели химии твердого тела, материаловедения и физики конденсированного состояния состоят в том, чтобы установить корреляцию между кристаллической структурой и физическими свойствами (Памплин, 1980; Канатзидис и др., 2005; Национальная академия наук инженерной медицины, 2009).Монокристаллические твердые частицы обеспечивают подходящую и простую платформу из-за отсутствия границ зерен и подавления и / или контроля дефектов. Большие, миллиметровые или даже более крупные монокристаллы незаменимы для характеристики анизотропных физических свойств, таких как магнитные, теплопередающие и зарядовые или оптические свойства (Phelan et al., 2012; Babu et al., 2018; Liu et al. ., 2018; Кэнфилд, 2020). Научное сообщество подняло высокие стандарты выращивания монокристаллов. Рост монокристаллов должен быть быстрым, контролируемым и способным работать со сложными системами (Pamplin, 1980; Kanatzidis et al., 2005; Национальная академия наук инженерной медицины, 2009 г .; Кэнфилд, 2020). Одним из вариантов является выращивание кристаллов из высокотемпературной расплавленной среды, флюса, который широко используется для выращивания различных интерметаллических, полупроводниковых и изоляционных соединений различной химической природы, от оксидов и галогенидов до металлических сплавов (Pamplin, 1980; Canfield, Fisk, 1991; Kanatzidis et al., 2005; Bugaris, zur Loye, 2012; Phelan et al., 2012; Juillerat et al., 2019; Canfield, 2020).Искусство выращивания кристаллов флюса – это сочетание науки и технологий. Научная часть требует всесторонних знаний о химической связи и реакционной способности компонентов и флюса в сочетании со знаниями термодинамики и кинетики процессов роста. Технологический аспект выращивания кристаллов заключается в методе «проб и ошибок», что требует нескольких попыток, иногда руководствуясь интуицией производителя. Исследования роста потока in situ предоставили понимание структуры жидкой фазы и каскадов превращений твердое тело в твердое, происходящих во время нагрева и охлаждения (Shoemaker et al., 2014; Woo et al., 2018). Некоторые общие аспекты выбора флюса, вместе с примерами и проблемами, обсуждаются в этой статье с акцентом на тройные и мультикомпонентные фосфиды и арсениды. Химия фосфидов и арсенидов при повышенной температуре усложняется из-за высокого давления пара P или As. Летучесть P и As привела к плохому изучению многих фазовых диаграмм металл-фосфор (мышьяк) в областях с высоким содержанием пниктогена. Тем не менее, соединения со значительным содержанием P (As) часто демонстрируют интересный химический состав и полезные практические свойства с потенциальными применениями в качестве теплопроводников, термоэлектриков, катализаторов и нелинейных оптических материалов (Soheilnia et al., 2007; Линдси и др., 2013; Долынюк и др., 2017; Nuss et al., 2017; Pöhls et al., 2017; Ли и др., 2018; Оуэнс-Бэрд и др., 2018, 2019; Woo et al., 2018; Coleman et al., 2019; Марк и др., 2019; Ю. и др., 2019).
Flux: общие соображения
Существуют различные варианты выращивания неорганических кристаллов с помощью флюса, например флюса металла, солевого флюса или собственного флюса. Основные соображения по выбору флюса включают три аспекта: растворимость реагентов во флюсе, путь реакции, а также зарождение и рост целевых кристаллов (рис. 1, внизу).Предположения о растворимости реагентов во флюсе в основном взяты из бинарных фазовых диаграмм (рис. 1G). Процесс роста кристаллов флюса обычно сопровождается химической реакцией, отличной от роста молекулярных соединений, где преобладают методы перекристаллизации. В большинстве случаев поток играет двойную роль в процессе роста кристаллов: облегчая химические реакции и способствуя росту кристаллов (рис. 1H, I). В дополнение к химическим и физическим свойствам реагентов и продуктов следует также учитывать взаимодействия между реагентами и флюсом.Контролировать зарождение и рост новой системы сложно из-за отсутствия систематических исследований. Для компенсации проводится серия экспериментов, в которых проверяются несколько соотношений флюс / реагент и скорости нагрева / охлаждения. Из-за ограниченного размера этого миниобзора подробные обсуждения термодинамики и кинетики здесь не рассматриваются.
Рисунок 1 . Вверху: Примеры кристаллов фосфида и арсенида, выращенных в различных потоках (Wang et al., 2013; Долынюк и др., 2015; Woo et al., 2018, 2019a). (D, F) показывают неопубликованные кристаллы, синтезированные в группе Ковнир. Внизу: основные аспекты роста кристаллов флюса. (A) BaCu 2 P 4 дюймов Sn, (B) Ba 3 Cd 2 As 4 дюймов Pb, (C) Mg 3 Si 6 As 8 дюймов Bi, (D) CeCd 3 P 3 дюймов KCl / NaCl, (E) CsZn 0,5 Si 5.5 As 12 в CsCl, (F) RbFe 2 As 2 в FeAs, (G) M-As фазовая диаграмма, (H) Твердотельная реакция, (I) Зарождение и рост.
Для изучения новой системы очень важно выбрать подходящий флюс. Следующие соображения относительно свойств флюса важны:
Растворимость
Требуются умеренная растворимость целевой фазы во флюсе и низкотемпературная зависимость растворимости.Низкая растворимость реагентов и целевой фазы предотвращает химические реакции и рост кристаллов. Однако очень высокая растворимость приведет к образованию ненасыщенных растворов, препятствующих кристаллизации целевой фазы. Температурная зависимость растворимости целевой фазы играет решающую роль в процессе роста кристаллов, поскольку она определяет скорость охлаждения. Для новой системы или нового соединения растворимость и ее температурная зависимость часто неизвестны и их нелегко определить, но несколько подсказок можно получить, проведя несколько модельных экспериментов.Скорость охлаждения составляла всего 0,4 К / ч, что потребовало недель для завершения роста.
Инертность
Инертность флюса необходима для предотвращения образования стабильных фаз между флюсом и реагентами. Образование соединений, содержащих флюс, изменит стехиометрию и нарушит процесс зародышеобразования. Другой аспект инертности флюса – нежелательное легирование целевой фазы компонентами флюса.
Температура плавления
Большой температурный диапазон идеален для выращивания кристаллов.Благоприятные флюсы имеют низкие температуры плавления в сочетании с высокими температурами кипения.
Токсичность
Нетоксичный флюс с низким давлением пара безопаснее и проще в обращении для окружающей среды и исследователей. Например, Hg редко используется в качестве флюса.
Контейнер
Чтобы избежать включения элементов контейнера в систему и / или целевых кристаллов, химические реакции между флюсом и контейнером крайне нежелательны. Если флюс имеет низкую растворимость летучих реагентов (P, As) или сам флюс имеет высокое давление пара, объем контейнера является другим параметром, который необходимо учитывать.
Удаление
Флюс следует удалить после завершения роста. Часто используются несколько методов, включая механическое разделение и полировку кристаллов, высокотемпературное центрифугирование жидкого флюса и растворение флюса при комнатной или близкой к ней температуре. В последнем случае природа флюса определяет, следует ли использовать простые растворители (вода, этанол) или кислоты (HCl, H 2 O 2 / уксусная кислота). Растворение требует, чтобы целевая фаза была стабильной в этой среде, что ограничивает выбор флюсов.Таким образом, KCl / NaCl предпочтительнее флюса Sn для чувствительных к кислоте материалов из-за растворимости хлоридов в воде. Флюсы Bi и Pb не растворяются в неокисляющих кислотах и требуют присутствия перекиси водорода в растворяющей среде.
Цена
Flux используется в больших количествах по сравнению с количествами целевых материалов или реагентов. Таким образом, очень дорогие флюсы всегда не лучший выбор, особенно при использовании подходов «проб и ошибок». Например, эвтектика Au / Si (T , плавление = 636 K) может быть хорошим флюсом, но она редко используется из-за высокой цены на золото.
Вязкость, плотность и полярность
Высокая вязкость флюса может привести к нестационарному массопереносу, который не приносит пользы для роста кристаллов. Плотности реагентов и флюса должны быть сопоставимы. Подобно смешиванию воды и бензола в химическом стакане, во время роста кристаллов флюса может происходить разделение фаз. В комбинации вода / бензол не только плотность, но и полярность жидкостей играет важную роль. Для синтеза флюсов, как показывает практика, металлические фазы лучше растут из металлических флюсов (Sn, Pb, Bi), в то время как полупроводниковые кристаллы легче выращивать из полупроводниковых флюсов (солей).Это не строгое правило, и исключения известны.
Суть в том, что ни один флюс не может удовлетворить всем критериям. Однако эти руководящие принципы могут помочь сделать рациональный выбор потока для синтеза.
Примеры металлических флюсов
Фосфор и мышьяк могут образовывать бинарные пниктиды почти со всеми металлами (кроме Hg и Bi) (Shatruk, 2019). Ртуть имеет высокое давление пара и токсична, поэтому висмут должен быть первым выбором для флюса для выращивания фосфидов и арсенидов, исходя из критериев инертности флюса.Bi хорошо подходит для арсенидов из-за относительно высокой растворимости As в Bi. Однако растворимость P в Bi довольно низкая, и для фосфидов предпочтительным является флюс Sn. Несмотря на существование ряда бинарных фаз Sn – P, из флюса Sn были выращены несколько сложных фосфидов (Kanatzidis et al., 2005). Фосфиды олова могут быть смыты кислотой и имеют умеренные точки плавления ниже 850 К. Бинарные арсениды олова имеют такие же температуры плавления, что и фосфиды олова, ~ 870 К; однако Sn имеет несколько ограниченный успех в качестве флюса для выращивания арсенидов; см. пример R Co 2 Pn 2 фаз ниже.Обычным побочным продуктом попыток выращивания арсенида в оловянном флюсе является бинарный SnAs со структурой NaCl, которая отличается от SnP. Последняя представляет собой метастабильную фазу с уникальной кристаллической структурой (Gullman, 1990). Требуются более систематические исследования, чтобы выяснить, является ли SnAs важным промежуточным продуктом, влияющим на процессы кристаллизации, или просто обычным побочным продуктом.
Недавно сообщалось, чтоPb образует бинарный PbP 7 (Schäfer et al., 2014), который демонстрирует более высокое сродство Pb к P по сравнению с Bi, несмотря на то, что точная фазовая диаграмма для системы Pb – P не сообщается.Свилен Бобев и др. сообщили о множественных успешных выращиваниях кристаллов как фосфидов, так и арсенидов из свинцового флюса (Bobev et al., 2009; Saparov, Bobev, 2010; He et al., 2016). Наконец, другие металлические флюсы, такие как Zn, Al, Ga и In, использовались для отдельных случаев роста кристаллов фосфидов и арсенидов.
BaCu
2 P 4 дюйм Sn ФлюсСинтез скрученного клатрата BaCu 2 P 4 (Долынюк и др., 2015) затруднен существованием другого клатрата близкого состава, BaCu 2 P 3.75 . Термический анализ подтвердил, что BaCu 2 P 4 превращается в BaCu 2 P 3,75 при нагревании перед плавлением, что объясняет экспериментальные наблюдения, что высокотемпературный синтез BaCu 2 P 4 всегда приводил к образование BaCu 2 P 3,75 . В свою очередь, исходные материалы Ba и Cu неактивны при низких температурах (<1000 K) из-за их высоких температур плавления, 1003 и 1353 K соответственно.Чтобы решить эту проблему, был применен рост потока. P имеет высокую растворимость в Sn (Завражнов и др., 2018), который может быть удален центрифугированием. Кристаллы BaCu 2 P 4 миллиметрового размера были успешно выращены с помощью флюса Sn при 1073 К (рис. 1A).
Mg
3 Si 6 As 8 In Bi FluxТрехкомпонентная система Mg – Si – As в течение многих лет игнорировалась только с одним теоретически предсказанным соединением MgSiAs 2 (Woo et al., 2018).Наши синтетические усилия обнаружили три новых тройных соединения: MgSiAs 2 , Mg 3 Si 6 As 8 и Mg 3 Si 3 As 8 (Woo et al., 2018; Wang et al., др., 2019). Было подтверждено, что MgSiAs 2 имеет структурный тип халькопирита, в то время как два других соединения кристаллизуются с новыми типами структур. Рост кристаллов системы Mg – Si – As является сложной задачей из-за сочетания высокого давления паров Mg и As и инертности Si при температурах реакции.Как обсуждалось выше, для арсенидов Bi предпочтительнее флюса Sn. Действительно, в потоке Bi были получены красные кристаллы Mg 3 Si 6 As 8 размером в миллиметр (рис. 1C).
Ba
3 Cd 2 As 4 дюймов Pb FluxПри исследовании синтеза Ba 3 Cd 2 As 4 (Wang et al., 2013) для выращивания кристаллов применялись флюсы Cd и Pb. Cd имеет умеренный рабочий диапазон между температурами плавления и кипения, 594 и 1038 K соответственно.Использование Cd в качестве самопотока сводило к минимуму возможность включения посторонних элементов. Недостатком флюса Cd было образование бинарной примеси Cd 3 As 2 . Мелкие кристаллы Ba 3 Cd 2 As 4 были выращены из флюса Cd с низким выходом. Более крупные кристаллы Ba 3 Cd 2 As 4 были выращены из флюса Pb. Pb имеет сравнимую температуру плавления и намного более высокую температуру кипения, чем Cd, 603 и 2023 К соответственно. Реагенты Ba, Cd и As обладают разумной растворимостью в Pb при повышенных температурах.Кристаллы Ba 3 Cd 2 As 4 размером Mm были выращены во флюсе Pb (рис. 1B).
RCo
2 Pn 2 (R = редкоземельный металл; Pn = P и As) в потоках Sn и BiВ трех вышеупомянутых примерах прямые реакции элементов дали поликристаллические образцы целевых фаз. Часто это не так, и флюс используется для преодоления высоких реакционных барьеров. Например, реакции чистого La, Co и P привели к смеси стабильных бинарных фосфидов, LaP и CoP / Co 2 P, которые не будут реагировать друг с другом, предотвращая образование тройных соединений La – Co – P.Поток Sn решает эти проблемы, приводя к кристаллам R Co 2 P 2 размером в миллиметр, что позволяет установить взаимосвязь между структурой и магнитными свойствами (Kovnir et al., 2010, 2011a, b; Kovnir et al. ., 2013; Thompson et al., 2014a; Tan et al., 2017). При переходе на изоструктурные арсениды флюс олова не смог образовать ни одной фазы R Co 2 As 2 . Вместо этого был успешно применен флюс Bi (Thompson et al., 2011, 2014b; Tan et al., 2016а, 2018). Подробные структурные характеристики показали, что Bi способен частично заменять катионы R 3+ , вероятно, из-за его трехвалентной природы (Thompson et al., 2011). Свидетельств включения Sn в кристаллы R Co 2 P 2 не обнаружено. Однако сообщалось, что двухвалентный Sn частично заменяет Ba 2+ в изоструктурных A Fe 2 As 2 сверхпроводниках ( A = Ba, K) (Mathieu and Latturner, 2009).
GeP в флюсах Sn и Bi
Включение компонентов металлического флюса в кристаллическую структуру является одной из причин отказа от некоторых флюсов. Элементарный Ge и P не будут реагировать друг с другом при температурах, при которых бинарный GeP стабилен, что требует применения флюса. Рост ван-дер-ваальсовых полупроводниковых кристаллов GeP производился из потока Sn (Lee et al., 2015). Подробные структурные характеристики показывают, что значительная степень беспорядка как в Ge, так и в P-узлах вносится частичной заменой Ge более крупными атомами Sn.Легирование Sn привело к резкому снижению температуры плавления / разложения на 228 K по сравнению с исходным GeP. Аналогичным образом, увеличение удельного электросопротивления более чем на порядок было обнаружено для GeP, легированного оловом. Нелегированный GeP был успешно синтезирован с использованием флюса Bi вместо Sn. Включение Bi не было обнаружено с помощью SEM / EDS и кристаллографических исследований (Lee et al., 2015).
Примеры роста кристаллов солевого флюса
Многие кристаллы неорганических пниктидов можно выращивать в солевых флюсах.Солевые потоки представляют собой высокотемпературные ионные жидкости (табл. 1). Солевой поток может быть инертным (NaCl / KCl) или реактивным (CsCl, AuCl, ZnCl 2 ). Огромным преимуществом солевого флюса является простота удаления промывкой растворителем, особенно водой. Из-за отсутствия знаний о растворимости элементов в солях выбор солевого потока является эмпирическим процессом до тех пор, пока не будут построены соответствующие фазовые диаграммы. Пример кристаллов CeCd 3 P 3 , выращенных в потоке инертной соли NaCl / KCl, показан на рисунке 1D.Для преодоления инертности переходного металла часто можно применять реактивные флюсы. Таким образом, Ba T 2 P 4 и Ba T 2 P 3.75 ( T = Cu, Ni, Au) могут производиться, начиная с T Cl или T Cl. 2 предшественников и избыток Ba (Ковнир и др., 2011; Fulmer et al., 2013a, b; Долынюк и др., 2015). Хлориды металлов служат источником элемента T за счет реакций Ba + 2 T Cl → BaCl 2 + 2 T .Одновременно смесь хлоридов бария и переходных металлов служит флюсовой средой.
Таблица 1 . Отобранные кристаллы фосфида и арсенида, выращенные из флюса.
Наконец, солевой флюс можно использовать для снижения реакционной способности реагента. Металлический Cs чрезвычайно реактивен, сложен в обращении и требует перчаточного бокса из-за его пирофорной природы. Вместо этого с комбинацией CsCl + Mg можно безопасно работать на воздухе. CsCl используется в качестве флюса и источника Cs при производстве смеси хлоридов Mg и Cs, которые удаляются промывкой водой после синтеза (рис. 1E) (Woo et al., 2019а).
La
2 Mg 3 SiP 6 дюймов MgI 2 ФлюсКак показано в Таблице 1, солевой поток был полезен для выращивания соединений в системах La– M –P ( M = Zn, Cd, Cu, Mg, Si). Росту кристаллов La 2 Mg 3 SiP 6 препятствовало сочетание инертности La и Si и высокой реакционной способности и давления паров Mg и P (Wang et al., 2017). Попытки выращивать La 2 Mg 3 SiP 6 с использованием металлического флюса Sn или Zn не увенчались успехом.Переход на флюс KCl / NaCl привел только к смеси Zn 3 P 2 и SiP 2 . Наконец, было доказано, что MgI 2 является подходящим флюсом для роста кристаллов La 2 Mg 3 SiP 6 . Частичное разложение MgI 2 при температурах реакции и выделение йода, который может служить транспортным агентом, может играть роль в повышении реакционной способности бинарных фосфидов.
Self-Flux
Рост кристалла за счет собственного потока (поток, состоящий исключительно из элементов, присутствующих в целевых кристаллах) имеет наименьшие шансы включения посторонних элементов.Самопотечение обычно предварительно синтезируется, примеры представлены в таблице 1. При исследовании синтеза тройной системы ABC все возможные бинарные соединения, AB, AC, BC, могут рассматриваться как самопотоки, если они соответствуют следующим критериям : легкий синтез, низкая температура плавления и высокая температура кипения, легкое удаление. Например, сверхпроводники Ca A Fe 4 As 4 ( A = K, Rb, Cs) изначально были обнаружены как поликристаллические образцы, которые существуют только в узком температурном окне (Iyo et al., 2016). После этого из самопотока FeAs были выращены крупные кристаллы (Meier et al., 2016). Особая конструкция тиглей, такая как тигли Кэнфилда, очень полезна для отделения крупных кристаллов от флюса (Canfield, 2020).
Транспортный рост в потоке
Транспортные реакции в жидком потоке имеют характерный температурный градиент. На горячем конце реагенты растворяются или образуют подвижные частицы, которые мигрируют к холодному концу и кристаллизуются в целевой фазе. Это означает эндотермическую равновесную реакцию, в то время как экзотермическую реакцию переносят от холодного конца к горячему.При условии, что температурный градиент является постоянным и включает температуру кристаллизации целевой фазы, рост кристаллов происходит на холодном конце с одновременным потреблением реагентов на горячем конце, аналогично реакциям переноса пара. Транспортные реакции не требуют полной растворимости реагентов во флюсе, что позволяет использовать более широкий выбор флюсов и более высокие массовые нагрузки исходных материалов, что приводит к получению большего количества кристаллов. Транспортные реакции допускают определенную гибкость при выборе флюса, поскольку растворимость реагентов может быть не столь критичной.В свою очередь, вязкость и связанный с ней массоперенос накладывают более строгие ограничения на выбор флюса. Этот метод является относительно новым, но был продемонстрирован для выращивания кристаллов антимонидов, галогенидов, халькогенидов и халькофосфатов переходных металлов с составами MP Q 3 ( Q = S, Se) (Yan et al., 2017). В настоящее время ведется разработка транспортных реакций для роста кристаллов фосфидов и арсенидов. Что касается переноса жидкости, предположительно, все ранее рассмотренные потоки могут позволить рост кристаллов, что указывает на то, что температурные градиенты могут быть полезной переменной при правильном применении.В более подробном обзоре Yan et al. (2017) продемонстрировали несколько примеров собственного потока и солевого потока, используемых для роста транспорта.
Обсуждение и перспективы
Как обсуждалось выше, у исследователя есть несколько методов на основе флюса для выращивания монокристаллов желаемых фосфидов и арсенидов. Не существует универсального, универсального метода флюса и нет гарантии, что для любого данного фосфида или арсенида может быть развит флюсовый рост кристаллов сантиметрового размера. Чтобы сделать последнее утверждение ложным, необходимы более систематические исследования механизмов роста потока.Поскольку реакция и рост кристаллов осуществляются в герметичной среде, чтобы сдерживать давление паров пниктогенов и предотвращать окисление воздухом, наблюдение за реакциями и процессами роста кристаллов ограничено. Необходимо сделать много предположений, основанных на простых двоичных фазовых диаграммах, которые не всегда верны, и не все двоичные фазовые диаграммы полностью разработаны. Вычислительное моделирование превращений жидкости в твердое тело в выбранных областях сложных фазовых диаграмм может помочь сократить количество попыток выращивания кристаллов.Недавние разработки методов in situ , ПЭМ и упругого рассеяния на синхротронных источниках и источниках нейтронов выявили множество скрытых процессов, происходящих во время синтеза потока, что позволило более рационально проектировать реакции потоков и рост кристаллов (Shoemaker et al., 2014 ; Woo et al., 2018, 2019b; Vasquez et al., 2019). Наконец, вычислительно дешевые методы, такие как машинное обучение (Yao et al., 2019), могут применяться для наведения мостов между методом проб и ошибок и полностью рациональными подходами.Результаты неудачных испытаний, которые документируются только в лабораторных журналах, необходимы для обучения моделей машинного обучения и выявления скрытых взаимосвязей.
Еще одна проблема, которую необходимо решить, – адаптивное управление ростом кристаллов. В настоящее время рост большей части кристаллов флюса основан на процессах самопроизвольной кристаллизации путем изменения температуры, начальных соотношений реагентов / флюсов и скорости охлаждения. Конструкция печи для выращивания кристаллов флюса нового типа, которая может уравновесить требования инертной атмосферы и контролируемый рост с помощью адаптивного контура обратной связи, может обеспечить кристаллы большего размера и лучшего качества.Последнее, что следует упомянуть, рост кристаллов флюса в экстремальных условиях, таких как высокая температура – высокое давление, остается практически неизученным. В связи с недавним открытием сверхпроводимости при почти комнатной температуре в супергидриде LaH 10 открываются широкие возможности для исследования новых фаз и механизмов реакций под действием приложенного давления (Geballe et al., 2018). Однако проблемы, связанные с наличием экстремальных условий и необходимостью работать в условиях ограниченного количества образцов, являются существенными.Кристаллы супергидридов пока не получены и не исследованы. Может быть, с помощью флюса при высоких температурах и под высоким давлением вырастут кристаллы супергидридов?
Авторские взносы
Рукопись написана при участии всех авторов. Все авторы одобрили окончательную версию рукописи.
Финансирование
Эта работа была поддержана Программой лабораторных исследований и разработок лаборатории Эймса в рамках контракта Министерства энергетики США №DE-AC02–07Ch21358.
Конфликт интересов
Авторы заявляют, что исследование проводилось при отсутствии каких-либо коммерческих или финансовых отношений, которые могут быть истолкованы как потенциальный конфликт интересов.
Благодарности
JW был благодарен за поддержку стартовым фондам Государственного университета Уичито. PY был благодарен программе стипендий Шатобриана.
Список литературы
Бабу Р., Гирибабу Л. и Сингх С. П. (2018).Последние достижения в области кристаллов перовскита на основе галогенидов и их оптоэлектронных приложений. Cryst. Рост Des. 18, 2645–2664. DOI: 10.1021 / acs.cgd.7b01767
CrossRef Полный текст | Google Scholar
Bao, J.-K., Liu, J.-Y., Ma, C.-W., Meng, Z.-H., Tang, Z.-T., Sun, Y.-L., et al. (2015). Сверхпроводимость в квазиодномерных K 2 Cr 3 As 3 со значительными электронными корреляциями. Phys. Ред. X. 5: 011013. DOI: 10.1103 / PhysRevX.5.011013
CrossRef Полный текст | Google Scholar
Бобев, С., Ся, С.-К., Бауэр, Э. Д., Роннинг, Ф., Томпсон, Дж. Д., и Саррао, Дж. Л. (2009). Дефицит никеля в RENi 2 − x P 2 (RE = La, Ce, Pr). Комбинированные исследования кристаллографических и физических свойств. J. Solid State Chem. 182, 1473–1480. DOI: 10.1016 / j.jssc.2009.03.014
CrossRef Полный текст | Google Scholar
Bugaris, D. E., and zur Loye, H.-C.(2012). Открытие материалов путем выращивания кристаллов флюса: оксиды четвертичного и высшего порядка. Angew. Chem. Int. Эд. 51, 3780–3811. DOI: 10.1002 / anie.201102676
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Кэнфилд П. К. и Фиск З. (1991). Выращивание монокристаллов из металлических флюсов. Philos. Mag. Б. 65, 1117–1123. DOI: 10.1080 / 136428115073
CrossRef Полный текст | Google Scholar
Ченг, Б., Ху, Б. Ф., Юань, Р. Х., Донг, Т., Фанг, А. Ф., Чен, З. Г. и др. (2012). Индуцированные полем спин-флоп переходы в монокристаллическом CaCo 2 As 2 . Phys. Ред. B 85: 144426. DOI: 10.1103 / PhysRevB.85.144426
CrossRef Полный текст | Google Scholar
Коулман Н. мл., Ловандер М. Д., Ледди Дж. И Гиллан Э. Г. (2019). Фосфиды металлов, богатые фосфором: прямой синтез и синтез с использованием флюса олова и оценка в качестве электрокатализаторов выделения водорода. Inorg.Chem. 58, 5013–5024. DOI: 10.1021 / acs.inorgchem.9b00032
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Долынюк Дж., Ван Дж., Ли К. и Ковнир К. (2015). Скрученные ячейки Кельвина и усеченные октаэдрические клетки в кристаллических структурах нетрадиционных клатратов, AM 2 P 4 (A = Sr, Ba, M = Cu, Ni). Chem. Матер. 27, 4476–4484. DOI: 10.1021 / acs.chemmater.5b01592
CrossRef Полный текст | Google Scholar
Долынюк, Ю., Заикина, Дж. В., Касеман, Д. К., Сен, С., и Ковнир, К. (2017). Нарушение правила тетракоординированной структуры: новый клатрат Ba 8 M 24 P 28 + δ (M = Cu / Zn). Angew. Chem. Int. Эд . 56, 2418–2422. DOI: 10.1002 / anie.201611510
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Фулмер, Дж., Касеман, Д., Долынюк, Дж., Ли, К., Сен, С., и Ковнир, К. (2013a). BaAu 2 P 4 : Многослойный полифосфид цинта с бесконечными (P – ) цепями. Inorg. Chem. 52, 7061–7067. DOI: 10.1021 / ic400584w
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Фулмер Дж., Лебедев О. И., Роддатис В. В., Касеман Д., Сен С., Долынюк Дж. И др. (2013b). Клатрат Ba 8 Au 16 P 30 : «Золотой стандарт» теплопроводности решетки. J. Amer. Chem. Soc. 135, 12313–12323. DOI: 10.1021 / ja4052679
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Гебалле, З.М., Лю, Х., Мишра, А. К., Ахарт, М., Сомаязулу, М., Мэн, Ю. и др. (2018). Синтез и стабильность супергидридов лантана. Angew. Chem. Int. Эд. 57, 688–692. DOI: 10.1002 / anie.201709970
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Хе Х., Стойко С., Бобев С. (2016). Новый взгляд на применение правил валентности в фазах Цинтля – Кристаллическая и электронная структура Ba 7 Ga 4 P 9 , Ba 7 Ga 4 As 9 , Ba 7 Al 4 Sb 9 , Ba 6 CaAl 4 Sb 9 и Ba 6 CaGa 4 Sb 9 . J. Solid State Chem. 236, 116–122. DOI: 10.1016 / j.jssc.2015.07.015
CrossRef Полный текст | Google Scholar
Иё, А., Кавасима, К., Киндзё, Т., Нишио, Т., Исида, С., Фуджихиса, Х., и др. (2016). Сверхпроводники на основе Fe новой структуры: CaAFe 4 As 4 (A = K, Rb, Cs) и SrAFe 4 As 4 (A = Rb, Cs). J. Am. Chem. Soc. 138: 3410. DOI: 10.1021 / jacs.5b12571
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Цзян, Дж., Олмстед, М., Каузларич, С. М., Ли, Х.-О., Клавинс, П., и Фиск, З. (2005). Отрицательное магнитосопротивление в магнитной полупроводниковой фазе Zintl: Eu 3 In 2 P 4 . Inorg. Chem. 44, 5322–5327. DOI: 10.1021 / ic0504036
CrossRef Полный текст | Google Scholar
Джуллера, К. А., Клепов, В. В., Моррисон, Г., Пейс, К. А., и Цур Лой, Х.-К. (2019). Выращивание кристаллов флюса: универсальный метод для раскрытия кристаллохимии сложных оксидов урана. Dalton Trans. 48, 3162–3181. DOI: 10.1039 / C8DT04675A
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Канатцидис, М. Г., Пёттген, Р., и Йейтчко, В. (2005). Металлический флюс: подготовительный инструмент для исследования интерметаллических соединений. Angew. Chem. Int. Эд. 44, 6996–7023. DOI: 10.1002 / anie.200462170
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ковнир К., Гарлеа В. О., Томпсон К. М., Чжоу Х.D., Reiff, W.M., Ozarowski, A., et al. (2011b). Поведение спинового стекла в твердых растворах LaFe x Co 2 − x P 2 : взаимодействие магнитных свойств, кристаллических и электронных структур. Inorg. Chem. 50, 10274–10283. DOI: 10.1021 / ic201328y
CrossRef Полный текст | Google Scholar
Ковнир К., Рейфф В. М., Менушенков А. П., Ярославцев А. А., Черников Р. В., Шатрук М. (2011a). Химический метамагнетизм »: от антиферромагнетика PrCo 2 P 2 до ферромагнетика Pr 0.8 Eu 0,2 Co 2 P 2 путем химического сжатия. Chem. Матер. 23, 3021–3024. DOI: 10,1021 / см200782z
CrossRef Полный текст | Google Scholar
Ковнир К., Штокерт У., Будник С., Проц Ю., Байтингер М., Пашен С. и др. (2011). Введение магнитного гостя в клатрат без тетрела: синтез, структура и свойства Eu x Ba 8 − x Cu 16 P 30 (0 ≤ x ≤ 1.5). Inorg. Chem. 50, 10387–10396. DOI: 10.1021 / ic201474h
CrossRef Полный текст | Google Scholar
Ковнир К., Томпсон К. М., Гарлеа В. О., Хаскель Д., Полянский А. А., Чжоу Х. и др. (2013). Модификация магнитной анизотропии через взаимодействие 3d-4f в La 0,75 Pr 0,25 Co 2 P 2 . Phys. Ред. B. 88: 104429. DOI: 10.1103 / PhysRevB.88.104429
CrossRef Полный текст | Google Scholar
Ковнир, К., Томпсон, К. М., Чжоу, Х. Д., Вибе, К. Р. и Шатрук, М. (2010). Настройка ферро- и метамагнитных переходов в фосфидах редкоземельного кобальта La 1 − x Pr x Co 2 P 2 . Chem. Матер. 22, 1704–1713. DOI: 10,1021 / см7h
CrossRef Полный текст | Google Scholar
Ли К., Синнестведт С., Беллард М. и Ковнир К. (2015). GeP и (Ge 1 − x Sn x ) (P 1 − y Ge y ) (x = 0.12, y = 0,05): синтез, структура и свойства двумерных слоистых тетрелфосфидов. J. Solid State Chem. 224, 62–70. DOI: 10.1016 / j.jssc.2014.04.021
CrossRef Полный текст | Google Scholar
Li, S., Zheng, Q., Lv, Y., Liu, X., Wang, X., Huang, P.Y., et al. (2018). Высокая теплопроводность в кубических кристаллах арсенида бора. Наука 361, 579–581. DOI: 10.1126 / science.aat8982
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Линдси, Л., Бройдо, Д. А., и Райнеке, Т. Л. (2013). Первопринципное определение сверхвысокой теплопроводности арсенида бора: конкурент алмазу? Phys. Rev. Lett. 111: 025901. DOI: 10.1103 / PhysRevLett.111.025901
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Лю С., Джо Г., Чжао Х., Чжоу Ю., Орвис Т., Хуян Х. и др. (2018). Гигантская оптическая анизотропия в квазиодномерном кристалле. Nat. Фотон. 12, 392–396. DOI: 10.1038 / s41566-018-0189-1
CrossRef Полный текст | Google Scholar
Марк, Дж., Ван, Дж., Ву, К., Ло, Дж. Дж., Ли, С., и Ковнир, К. (2019). Ba 2 Si 3 P 6 : 1D нелинейно-оптический материал с цепями термобарьера. J. Amer. Chem. Soc. 141, 11976–11983. DOI: 10.1021 / jacs.9b04653
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Матье, Дж. Л., и Латтурнер, С. Э. (2009). Фаза цинта как источник легирующей примеси при синтезе потока Ba 1 − x K x Fe 2 As 2 сверхпроводники типа . Chem. Commun. 33, 4965–4967. DOI: 10.1039 / b9e
CrossRef Полный текст | Google Scholar
Мейер, В. Р., Конг, Т., Калуараччи, США, Тауфур, В., Джо, Н. Х., Драчак, Г. и др. (2016). Анизотропные термодинамические и транспортные свойства монокристаллического CaKFe 4 As 4 . Phys. Ред. B 94: 064501. DOI: 10.1103 / PhysRevB.94.064501
CrossRef Полный текст | Google Scholar
Нусс, Дж., Ведиг, У., Се, В., Йорданов, П., Бруин, Дж., Хюбнер, Р. и др. (2017). Фосфид-тетраэдрит Ag 6 Ge 10 P 12 : термоэлектрические характеристики давно забытого соединения кластера серебра. Chem. Матер. 29, 6956–6965. DOI: 10.1021 / acs.chemmater.7b02474
CrossRef Полный текст | Google Scholar
Оуэнс-Бэрд, Б., Коленько, Ю.В., Ковнир, К. (2018). Зависимость структура-активность для электрокатализаторов выделения водорода из фосфидов металлов, не содержащих платины. Chem. Europ. J. 24, 7298–7311. DOI: 10.1002 / chem.201705322
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Оуэнс-Бэрд, Б., Сюй, Дж., Петровых, Д. Ю., Бондарчук, О., Зиуани, Ю., Гонсалес-Баллестерос, Н., и др. (2019). NiP 2 : история двух расходящихся полиморфных многофункциональных материалов. Chem. Матер. 31, 3407–3418. DOI: 10.1021 / acs.chemmater.9b00565
CrossRef Полный текст | Google Scholar
Одзава, Т.К., и Каузларич, С. М. (2003). Выращивание монокристаллов из потока (NaCl) / (KCl) и кристаллическая структура нового четвертичного смешанного металлического пниктида: BaCuZn 3 As 3 . Inorg. Chem. 42, 3183–3186. DOI: 10.1021 / ic034061k
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Памплин, Р. Б. (1980). Рост кристаллов, 2-е издание . Вашингтон, округ Колумбия: Pergamon Press.
Фелан, В. А., Менар, М. К., Кангас, М. Дж., МакКэндлесс, Г.Т., Дрейк, Б. Л., и Чан, Дж. Ю. (2012). Приключения в выращивании кристаллов: синтез и характеристика монокристаллов сложных интерметаллических соединений. Chem. Матер. 24, 409–420. DOI: 10,1021 / см2019873
CrossRef Полный текст | Google Scholar
Pöhls, J.-H., Faghaninia, A., Petretto, G., Aydemir, U., Ricci, F., Li, G., et al. (2017). Фосфиды металлов как потенциальные термоэлектрические материалы. J. Mater. Chem. С 5, 12441–12456. DOI: 10.1039 / C7TC03948D
CrossRef Полный текст | Google Scholar
Сапаров, Б., и Бобев, С. (2010). Изолированные бесконечные цепи [ZnPn2] ∞14− в фазах Zintl Ba 2 ZnPn 2 (Pn = As, Sb, Bi) – Синтез, структура и связывание. Inorg. Chem. 49, 5173–5179. DOI: 10.1021 / ic100296x
CrossRef Полный текст | Google Scholar
Шефер К., Бенндорф К., Эккерт Х. и Пёттген Р. (2014). PbP 7 – полифосфид с трехмерной [P 7 ] 2−− сеткой из конденсированных и P-мостиковых P 6 шестиугольников. Dalton Trans. 43, 12706–12710. DOI: 10.1039 / C4DT01539H
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Шатрук, М. (2019). «Синтез фосфидов», в Основы и применения фосфорных наноматериалов, Серия симпозиумов ACS , изд. Х. Джи (Вашингтон, округ Колумбия: Американское химическое общество), 103–134.
Google Scholar
Shoemaker, D. P., Hu, Y.-J., Chung, D. Y., Halder, G.J., Chupas, P.J., Soderholm, L., et al.(2014). In situ исследования платформы для роста метастабильных неорганических кристаллов и открытие материалов. Proc. Natl. Акад. Sci. США 111, 10922–10927. DOI: 10.1073 / pnas.1406211111
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Soheilnia, N., Xu, H., Zhang, H., Tritt, T. M., Swainson, I., and Kleinke, H. (2007). Термоэлектрические свойства Re 3 Ge 0,6 As 6,4 и Re 3 GeAs 6 по сравнению с Mo 3 Sb 5.4 Te 1,6 . Chem. Матер. 19, 4063–4068. DOI: 10,1021 / см0708517
CrossRef Полный текст | Google Scholar
Табассум, Д., Лин, X., и Мар, А. (2015). Редкоземельные арсениды марганца RE 4 Mn 2 As 5 (RE = La – Pr). J. Alloys Compd. 636, 187–190. DOI: 10.1016 / j.jallcom.2015.02.145
CrossRef Полный текст | Google Scholar
Тан, X., Фаббрис, Г., Хаскель, Д., Ярославцев, А.А., Цао, Х., Томпсон, К. М. и др. (2016a). Переход от локализованного к сильно коррелированному поведению электронов и смешанной валентности, вызванный физическим или химическим давлением в ACo 2 As 2 (A = Eu, Ca). J. Amer. Chem. Soc. 138, 2724–2731. DOI: 10.1021 / jacs.5b12659
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Тан X., Гарлея В. О., Чай П., Геонджян А. Ю., Ярославцев А. А., Синь Ю. и др. (2016b). Синтез, кристаллическая структура и магнетизм A 2 Co 12 As 7 (A = Ca, Y, Ce – Yb). J. Solid State Chem. 236, 147–158. DOI: 10.1016 / j.jssc.2015.08.038
CrossRef Полный текст | Google Scholar
Тан X., Гарлеа В. О., Ковнир К., Томпсон К. М., Сюй Т., Цао Х. и др. (2017). Сложная магнитная фазовая диаграмма с многоступенчатыми спин-флоп переходами в La 0,25 Pr 0,75 Co 2 P 2 . Phys. Ред. B , 95: 024428. DOI: 10.1103 / PhysRevB.95.024428
CrossRef Полный текст | Google Scholar
Тан, X., Тенер, З.П., Шатрук, М. (2018). Корреляция блуждающего магнетизма в R Co 2 Pn 2 пниктидов ( R = La, Ce, Pr, Nd, Ca, Pn = P, As) с их кристаллической и электронной структурой. В соотв. Chem. Res. 51, 230–239. DOI: 10.1021 / acs.accounts.7b00533
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Национальные академии наук, инженерная медицина (2009). Границы кристаллической материи от открытий до технологий .Вашингтон, округ Колумбия: The National Academies Press.
Google Scholar
Томпсон, К. М., Ковнир, К., Эвеланд, С., Херринг, М. Дж., И Шатрук, М. (2011). Синтез арсенидов типа ThCr 2 Si 2 из флюса Bi. Chem. Commun. 47, 5563–5565. DOI: 10.1039 / c1cc10578g
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Томпсон, К. М., Ковнир, К., Гарлеа, В. О., Чой, Э. С., Чжоу, Х. Д., и Шатрук, М. (2014a). Нетрадиционный магнетизм в ThCr 2 Si 2 -тип фосфидов, La 1 − x Nd x Co 2 P 2 . J. Mater. Chem. С. 2, 756–7569. DOI: 10.1039 / C4TC00564C
CrossRef Полный текст | Google Scholar
Томпсон, К. М., Тан, X., Ковнир, К., Гарлея, В. О., Гиппиус, А. А., Ярославцев, А. А. и др. (2014b). Синтез, структура и магнитные свойства арсенидов редкоземельного кобальта, RCo 2 As 2 (R = La, Ce, Pr, Nd). Chem. Матер. 26, 3825–3837. DOI: 10,1021 / см501522v
CrossRef Полный текст | Google Scholar
Васкес, Г., Хук, А., Латтурнер, С. Э. (2019). In situ нейтронографические исследования роста потока металла интерметаллидов Ba / Yb / Mg / Si. Inorg. Chem. 58, 8111–8119. DOI: 10.1021 / acs.inorgchem.9b00857
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ван Дж., Гринфилд Дж. Т. и Ковнир К. (2017). Синтез, кристаллическая структура и магнитные свойства R 2 Mg 3 SiPn 6 (R = La, Ce, Pn = P, As). Inorg.Chem. 56, 8348–8354. DOI: 10.1021 / acs.inorgchem.7b01015
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ван Дж., Ли К. и Ковнир К. (2015). Искаженные квадратно-плоские слои фосфора и меди в LaCu 1 + x P 2 и LaCu 4 P 3 : синтез, кристаллическая структура и физические свойства. Inorg. Chem. 54, 890–897. DOI: 10.1021 / ic502234w
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ван, Дж., Марк, Дж., Ву, К. Э., Войлс, Дж., И Ковнир, К. (2019). Химическая гибкость мг в пниктидных материалах: разнообразие структур и свойств. Chem. Mater . 31, 8286–8300. DOI: 10.1021 / acs.chemmater.9b03740
CrossRef Полный текст | Google Scholar
Ван, Дж., Ся, С.К., и Тао, X-Т. (2013). Синтезы, кристаллическая структура и физические свойства новых фаз цинка Ba 3 T 2 As 4 (T = Zn, Cd). J. Solid State Chem. 198, 6–9.DOI: 10.1016 / j.jssc.2012.09.029
CrossRef Полный текст | Google Scholar
Ван Дж., Йокс П., Войлс Дж. И Ковнир К. (2018). Синтез, кристаллическая структура и свойства трех соединений La – Zn – P с разной размерностью каркаса Zn – P. Cryst. Рост Des. 18, 4076–4083. DOI: 10.1021 / acs.cgd.8b00445
CrossRef Полный текст | Google Scholar
Ву К., Ли К. и Ковнир К. (2016). БП: синтез и свойства фосфида бора. Mater. Res. Expr. 3: 074003. DOI: 10.1088 / 2053-1591 / 3/7/074003
CrossRef Полный текст | Google Scholar
Ву, К. Е., Долынюк, Дж., И Ковнир, К. (2019a). Замена ван-дер-Ваальса электростатическими взаимодействиями: внедрение Cs в межслоевое пространство SiAs 2 . Inorg. Chem. 58, 4997–5005. DOI: 10.1021 / acs.inorgchem.9b00017
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ву, К. Э., Ван, Дж., Марк, Дж., И Ковнир, К. (2019b). Направление бор-фосфорных связей в кристаллическом твердом теле: окислительная полимеризация мономеров P = B = P в одномерные цепи. J. Amer. Chem. Soc. 141, 13017–13021. DOI: 10.1021 / jacs.9b06803
CrossRef Полный текст | Google Scholar
Woo, K. E., Wang, J., Wu, K., Lee, K., Dolyniuk, J.-A., Pan, S., et al. (2018). Mg-Si-As: неизученная система с многообещающими нелинейно-оптическими свойствами. Adv. Функц. Матер. 28: 180158. DOI: 10.1002 / adfm.201801589
CrossRef Полный текст | Google Scholar
Ян, J.-Q., Сейлз, Б.С., Суснер, М.А., и Макгуайр, М.А. (2017). Рост потока в горизонтальной конфигурации: аналог роста переноса пара. Phys. Rev. Mater. 1: 023402. DOI: 10.1103 / PhysRevMaterials.1.023402
CrossRef Полный текст | Google Scholar
Yao, T.-S., Tang, C.-Y., Yao Yang, M., Zhu, K.-J., Yan, D.-Y., Yi, C.-J., et al. (2019). Машинное обучение для инструктирования роста монокристаллов методом флюса. Подбородок. Phys. Lett. 36: 068101. DOI: 10.1088 / 0256-307X / 36/6/068101
CrossRef Полный текст | Google Scholar
Yu, T., Wang, S., Zhang, X., Li, C., Qiao, J., Jia, N., et al. (2019). MnSiP 2 : новый тройной фосфид среднего ИК-диапазона с сильным эффектом ГВГ и сверхшироким диапазоном прозрачности. Chem. Матер. 31, 2010–2018. DOI: 10.1021 / acs.chemmater.8b05015
CrossRef Полный текст | Google Scholar
Завражнов А.Ю., Семенова Г.В., Проскурина Е.Ю., Сушкова Т.П. (2018). Фазовая диаграмма системы Sn – P. J. Therm. Анальный. Калорим 134, 475–481. DOI: 10.1007 / s10973-018-7123-0
CrossRef Полный текст | Google Scholar
Том 56, страницы 1319-1331, 1971 МЕДНО-НИКЕЛЕВЫЕ АРСЕНИДЫ МОХАВКА № 2 МОЗА, МОЗАВК, KEWEENAW CO., Мичиган ПОЛ Б. МУР, Департамент геофизических наук, Университет из Чикаго, Чикаго, Иллинойс 60637 Аннотация Арсениды никеля меди, собранные из большой трещины на могавке No.2 мой, Mohawk, Keweenaw Co., штат Мичиган, были исследованы методом порошковой дифрактометрии и электронно-зондовый анализ. Эти материалы соответствуют «кевинавиту». и «могавкит» Кенига и «ледуксит» Ричардса. Выявленные фазы включают α-домейкит, β-домейкит, альгодонит, мышьяк. медь, раммельсбергит, парараммельсбергит и никколит. Исследования герметичных кварцевых трубок в системе Cu-Ni-As при 510 ± 5 ° C показывают незначительные растворимость меди в арсенидах никеля и никеля в арсенидах меди.Все примеры, встречающиеся в группе неравновесных могавков, по-видимому, по существу не содержат твердой растворимости (Cu, Ni) среди бинарных арсенидов. соединения. Имеются убедительные доказательства того, что арсениды никеля кристаллизовались раньше всего. более высокой температуры, были разрушены и впоследствии частично заменены растворы, содержащие арсенид меди при более низкой температуре. Оправы реакции вокруг арсениды никеля представляют собой продукты, которые соответствуют предполагаемым стабильность сосуществующих фаз в системе Cu-Ni-As. ВВЕДЕНИЕ В этой статье описывается и обсуждается парагенезис сосуществующих медно-никелевые арсениды, которые включают так называемый «кевинавит» и «могавкит» шахты «Ирокез № 2», Мохок, Кевинау, штат Мичиган. До появления методов металлографии и рентгеновской дифрактометрии, в литературе появилось множество имен, в том числе «ледуксит» (Richards, 1901), «кевинавит», «ирокез» и «уитнейт» (Кениг, 1900).В конечном итоге было заявлено, что все они являются смесями по крайней мере семи известных и неизвестных фаз Батлера и Бербанка (1929). Хотя эти авторы в первую очередь обсуждали арсениды меди, они упомянули существование нескольких неизвестных арсенидов никеля и кобальта. Теперь недоступный вал ирокез № 2 был вбит в член Серия Kearsarge Lode из миндалевидного базальта и обнаружила необычно большие количества арсенидов меди, о чем свидетельствует удаление более 230000 фунтов материала «ирокит» (Батлер и Бербанк, 1929).Более свежий список медно-никелевых арсенидов из этого региона был опубликован Уильямсом (1963). Сосуществующие арсениды меди и никеля встречаются редко и включают Cerý, Dul, Крконоше, Богемия, где мышьяк, арсеноламприт, никколит, коутекит, паксит и новакит были описаны Йохан (1962) и месторождение Талмесси, Анорак, Иран, откуда никколит, альгодонит и α-домейкит были идентифицированы Бариандом и Херпином (1960). Чтобы помочь в парагенетической интерпретации арсенидов шахты могавк, Система Cu-Ni-As исследована при 510 ± 5 ° C путем синтеза в вакуумированном герметичном кремнеземные трубки. АРСЕНИДЫ МОЗАВКА № 2 ШАХТА Обнаруженные и описанные фазы включают α-домейкит (Cu 3 As), β-домейкит. (Cu 3-x As), альгодонит (Cu 6 ± x As), мышьяковая медь (Cu, As) н.в. , раммельсбергит (NiAs 2 ), парараммельсбергит (NiAs 2 ) и никколит (Ni 1 ± x As). Образцы . Репрезентативная серия образцов была собрана в 1962 г. автор с 11-го и 12-го уровней, 200 футов С.W. вала могавка № 2. С тех пор доступ к стволу был закрыт, и соседние шахты с подъездные пути были заброшены. Арсенидсодержащая трещина защемления и вздутия, в некоторых местах достигая толщиной четыре фута и почти полностью заполнен арсенидами и значительные количества почти чистого кальцита. Недавние действия минных вод произвел многочисленные гидратированные арсенаты кальция и меди, которые часто покрывают кальцит и арсениды.В некоторых местах кальцит является единственным минералом. А История брекчии очевидна по угловатым кускам стеновой скалы, погруженным в внутри кальцита. Большой забой между уровнями обнажает трещину, которая показаны жилы α-домейкита толщиной до двух футов. Материал на месте бледного халькопиритово-желтого цвета, внешне напоминающего пирротин; когда только что сломанные образцы издают запах арсинового газа. Когда доведен до поверхность, α-домейкит обычно тускнеет до желто-халькопиритового цвета и в течение нескольких лет образует нечеткое черное порошкообразное покрытие, не заметное в situ , который состоит как минимум из двух фаз.Одна из этих фаз бледно-зеленая в цвет и дает сложный порошковый узор, похожий на тиролит, что указывает на продукт окисления. Это покрытие наблюдается практически на всех α-домейкитах. сохранились в коллекциях. Вполне вероятно, что наличие восстановительных шахтных газов такие как метан, ингибируют поверхностное окисление α-домейкита на месте. Сучки серовато-оловянно-белого раммельсбергита ботриоидно-волокнистого вида возникают в местах, обычно по краю трещины, и эти неизменно показаны древовидные трещины, заполненные α-домейкитом.Полированные изделия из “кевинавита” показать раммельсбергит с почковидными или ботриоидными очертаниями, имитирующими появление арсенидов кобальт-никеля из региона Кобальт-Садбери в Онтарио. Масса до шести дюймов в диаметре, состоящая в основном из никеля. арсениды не редкость, но α-домейкит является самым распространенным арсенид в трещина. Розоватый никколит обычно отделяет раммельсбергит от α-домейкита. и происходит от тонких зон до довольно больших масс, тесно смешанных с раммельсбергит и α-домейкит. Часто в центрах заполнения трещин присутствует α-домейкит, проходящий через латерально в смеси α-домейкита и никколита, которые, в свою очередь, переходят в никколит-раммельсбергитовые смеси. На рисунке 1 представлен типичный внешний вид и показаны древовидный α-домейкит, окаймленный никколитом, примыкающим к раммельсбергиту. Эти фазы можно визуально различить, если разрешены шлифовки. тускнеть на воздухе. Раммельсбургит сохраняет свой оловянно-белый вид, никколит выглядит медно-розовым, а α-домейкит приобретает маслянисто-зеленый налет.Иногда эти смеси настолько тщательно перемешаны, что разделение фаз недопустимо. – даже зондовой техникой – и необходимо прибегать к порошковой дифрактометрии. Хотя соседние большие массы α-домейкита, по-видимому, состоят из чистый материал, редкие крошечные остаточные зерна никколита, мышьяковистой меди и альгодонита были проверены с помощью зондового анализа. Рис. 1. Фотография смеси α-домейкит-раммельсбургит-никколит, которая была отполированы и позволили потускнеть на воздухе.Α-домейкит выглядит как темное дерево. нравиться очертания, а смесь никколит-раммельсбергит крапчатый. Редкие острова чистый раммельсбергит белые. Кальцит, окружающий образец и который происходит как редкая поздняя стадия вены белого цвета. Образец около 5 см. через. Эти смеси раммельсбергит-никколит-α-домейкит обнаруживают поразительное сходство к типовым образцам «кевинавита» и «ирокита» Кенига которые он, по-видимому, собрал из той же трещины, пересекающей 5-й уровень, и интимный аспект некоторых смесей несомненно привел его к заключению что материалы были однородными.Местоположение Кенига было недоступно во время время сбора образцов из-за обширного обрушения шахты. Менее частые виды, идентифицированные в ходе этого исследования, включают: парараммельсбергит, β-домейкит, альгодонит и мышьяковистая медь. В альгодонит и мышьяковистая медь, редко встречающиеся в этом местонахождении, чаще встречаются на некоторые другие шахты. Огромные массы когда-то были встречены на Ахмике № 3. и 4 шахты примерно в миле к югу, и теперь они лежат в кучах отходов.В β-домейкит обычно смешан с α-домейкитом; однако образец собраны и любезно подарены Г. Куллерудом из соседней шахты Сенека состоит в основном из β-домейкита. Маучерит не встречался, но он встречается в некоторых трещинах в других местах на полуострове Кевинау, обычно с альгодонитом (Р. Дж. Скиннер, личное сообщение). Можно отметить, что относительные содержания фаз Cu-Ni-As встречающиеся даже в одной трещине, могут сильно различаться, и совокупность, описанная здесь, является представитель только в одном конкретном месте.Однако считается, что детальный микропарагенез ассоциированных фаз по существу повторяется на другие находки арсенида на полуострове Кевинау с тех пор, как образцы арсениды меди и никеля из нескольких других мест показывают то же самое ассоциации при рассмотрении в малом масштабе. Экспериментальная . Электронно-зондовый анализ ARL и исследования порошковой рентгеновской дифракции были предприняты на природных образцах. Исследования в системе Ni-As, Юнд (1961) и система Cu-As Скиннера, Адлера и Мида (1963), а также Скиннера и Люс (1971) и изотермический разрез системы Cu-Ni-AS при 510 ° C, обсуждаемые впоследствии, были неоценимыми помощниками в толковании минералогические отношения. Объемный анализ падений “кевинавита” и “ирокита” Кенигом в поле Cu 3 As-NiAs 2 -Ni 11 As 8 , как показано на рисунке 2 и образцы исследуемые в этой статье, за редким исключением, также подпадают под эту область. На электронном зонде были выполнены два вида анализа. Поглощение матрицы и Расчеты усиления показали, что поправки не требуются, если чистая Cu 3 As и NiAs 2 использовались как стандарты.К ним относятся химически проанализированный α-домейкит и раммельсбергит, последний содержит 0,6% Со. кобальт в раммельсбергите в качестве стандартов представляет собой стехиометрические и чистые соединения. Используя На пучке 2 мкм снимались спектры CuKα, NiKα и AsKα. проанализированы. Рис 2. Образцы “могавкита” и “кевинавита”, которые были проанализированы. Кенига (1960) объемные анализы включают «могавкит» (M) и «кевинавит». (К).Анализы от a до i представлены в таблице 1. Таблица 1. Электронный зонд Микроанализ медно-никелевых арсенидов могавка
Первая серия анализов была основана на полированном срезе по существу чистый α-домейкит, составлявший часть больших масс арсенида (табл. к г) и полированный срез «кевинавита» (таблица 1, е-i). Результат анализы показаны на рисунке 2.Второй набор анализов состоял из пересекает прожилки α-домейкита, секущие раммельсбергит и никколит, и эти результаты показаны на рисунке 3. Порошковые дифрактограммы были получены для ряда “кевинавита”. и образцы “ирокита” с использованием излучения Cu с фильтром Ni и CaF 2 в качестве внутреннего стандарта. Эти все смеси содержали различные количества раммельсбергита, никколита, α-домейкита, β-домейкит и парараммельсбергит.Два типичных дифракционных спектра образцы из второго набора зондового анализа представлены в таблице 2. расстояния были проиндексированы в соответствии с ориентацией ячеек, представленной в ASTM. Файл данных по пороху, 1963 г. Образец, состоящий из неравновесной ассоциации парараммельсбергита, никколит и α-домейкит были тонко измельчены и нагреты в герметичной кремнеземной трубке. в течение семи дней в 510 ± 5 ° C в попытке определить верхний предел температура инверсии парараммельсбергита.Отделение парараммельсбергита от соседство никколита и α-домейкита было недопустимо, так как ассоциация была очень смешанной. Однако изучение система Cu-Ni-As демонстрирует, что присутствие арсенидов меди и никколит практически не повлияет на температуру инверсии стехиометрическая диморфная пара NiAs 2 . В появление раммельсбергита после нагревания (таблица 3) показывает, что температура инверсии диморфной пары равна понижен в материале ирокез, поскольку Юнд установил эту инверсию для чистые соединения при 590 ± 10 ° C и давлении 1 бар путем экстраполяции в пространство P-T.С некоторые другие переходные элементы и элементы групп V и VI известны как сильно влияют на температуру инверсии арсенидов, даже если они присутствуют в относительно небольшие количества, считается, что присутствие кобальта в Материал ирокез способствовал снижению температуры инверсии. Чрезвычайная инверсия при более низких температурах запрещена. определение нижнего предела температуры. Рис 3.Электронный микрозонд ARL пересекает “keweenawites” интерпретируется как массовые проценты. Кресты падают с чистых композиционных линий представляют собой мелкодисперсные механические смеси Примечание о субсолидусе Cu-Ni-As при 510 ± 5ºC Основная цель этого эксперимента состояла в том, чтобы установить степень твердого раствор никеля в арсенидах меди и меди в арсенидах никеля, возможное существование какой-либо тройной фазы или фаз и полей сосуществующих фаз.Реакции протекают относительно быстро при температуре около 500 ° C и, поскольку некоторые из фаз, относящихся к неравновесному комплексу могавков, сохраняются для этой температуры была выбрана эта изотерма. Следует подчеркнуть, что природные комплексы депонированы на более низкие температуры и содержат бинарные фазы, отсутствующие в этой изотермической система. Хотя ограниченная растворимость твердых веществ в ионной системе при более высокой температуре указывает на еще меньшую растворимость при некоторой более низкой температуре, тот же вывод применяется к ковалентно связанным системам, таким как арсениды, должен использоваться с осторожность, поскольку состояния электронной зоны чувствительны к температуре.Мы заметили, однако, по всей видимости, не существует какой-либо изотипической пары в Cu-As и Системы Ni-As даже при низких температурах, в пользу вывода о вероятном отсутствии растворимости твердых веществ, если так обстоит дело при более высоких температурах. Таблица 2. Рентгеновская порошковая дифрактография смесей «Кевинавита». Cu / Ni излучение, CaF 2 внутренние, погрешности ± 0,003Å
Рис. 4. Интерпретация конденсированной системы Cu-Ni-As при 510 ° С. В пробеги перечислены в Таблице 4. Экспериментальный Никель, содержащий менее 0.03% примесей и меди и мышьяк, каждый с содержанием примесей менее 0,002%. Все в экспериментах использовались вакуумированные и герметичные пробирки из кварцевого стекла со стеклянным стержнем. вставлен плотно упаковать заряд и минимизировать паровое пространство. Заряды нагревали при 510 ± 5 ° С в течение десяти суток, повторно измельчить для обеспечения равномерного перемешивания, запечатать и нагреть еще шесть дней, охладить капнув в ледяную воду , а затем исследовали оптически на предмет неоднородностей. Материалы во всех эксперименты, похоже, отреагировали быстро и полностью.Фазы присутствуют были идентифицированы традиционными методами порошковой дифракции колебаний, с использованием CaF 2 ( a = 5,4626 ± 0,0005Å) в качестве внутреннего стандарта.Наличие фаз . Следующие твердые фазы были синтезированы в этих эксперименты: твердый раствор медь-никель-мышьяк (Cu, Ni, As) s.s. , г. β-домейкит (β-дом, Cu 3-x As), коутекит (ko, Cu 5 As 2 ), парараммельсбергит (prm, NiAs 2 ), никколит (nc Ni 1 ± x As) и маучерит (ma, Ni 11 As 8 ).Существенные особенности конденсированная система Cu-Ni-As при 510 ° C показана на Рисунке 4; в соответствующие сборы перечислены в Таблице 4.На этом изотермическом разрезе тройные фазы не встречались. К одновариантным полям относятся (As, Cu) с.с. + ko + prm + Vapor (V) 1 ; ко + β-дом + прм + V; прм + нк + β-дом + V; nc-ma + β-dom + V; ma + Ni 5-x As 2 + β-dom + V; (Cu, Ni, As) s.s. + Ni 5-x As 2 + βdom + V.Дивариантные поля представлены двумя тонкими полосками nc s.s. + β-dom + V и β-дом s.s. + (Cu, As, Ni) н.в. + V; и обширный (Cu, Ni, As) s.s. + Ni 5-x As 2s.s. + V поле.Note1 Давление паров мышьяка не превышает 1 Атм. ниже 604 ° C. Таблица 3. Порошковая рентгеновская дифрактография необогреваемого и нагретого могавка Парараммельсбергит. Излучение Cu / Ni, CaF 2 внутренняя, погрешность ± 0.003Å.
Таблица 4.Синтезы в Система Cu-Ni-As при 510 ± 5 ° C В этом исследовании показано, что парараммельсбергит является стабильным диморфом и сделан вывод, что присутствие сосуществующих арсенидов меди имеет мало или совсем не влияет на температуру инверсии. Колебательные дифрактографы о отражении d 121 синтетического парараммельсбергита, сосуществующего с β-домейкит приготовлено при 510 ° C, а также d 111 из раммельсбергит сосуществует с β-домейкит при 650 ° C не показывают значительных различий в их соответствующих интервалах d , когда по сравнению с чистым синтетическим NiAs 2 диморфов (Таблица 5). Таблица 5, Рентгеновская порошковая дифрактография синтетического и монвкского раммельсбергита, Парараммельсбергитовые, никколитовые, α-домейкитовые комплексы. Cu / Ni излучение, CaF 2 внутренний, погрешности ± 0,003 Å
Коутекит, Cu 5 As 2 , является стабильной фазой арсенида меди в богатый мышьяком часть диаграммы и сосуществует с парараммельсбергитом мышьяка и β-домейкит.В системе Cu-Ni-As при 510 ° C коутекитсодержащие поля представлены обширным ko + As s.s. + prm + V и поле тонкая полоска кот + β-дом + прм + в. Таким образом, коутекит не сосуществует с никколитом или маучерит. От NiAs 2 -Cu 5 As 2 присоединяется к Ni 5-x As 2 (x ~ 0,2) – (Cu, Ni, As) с.н. присоединиться, β-домейкит – стойкая фаза Cu-As. Альгодонит (Cu 6 ± x As) не встречался, так как он разлагается при температурах выше 300 ± 20 ° C с составом Cu 8 Что касается β-домейкит + Cu с.с. и α-домейкит отсутствовал, так как он разлагается при температурах выше 90 ° C до альгодонита и дефицита меди β-домейкит, согласно Скиннеру и Люси.Предполагается, что никель не играет существенной роли в разложении и температуры инверсии низкотемпературных арсенидов меди, поскольку существенно отсутствие растворимости твердого никеля в Обнаружен β-домейкит и коутекит при 510 ° C. Действительно, электронно-зондовый анализ естественно наличие низкотемпературных сосуществующих фаз Ni-As и Cu-As не давало никаких доказательства обнаружения никеля в арсенидах меди или меди в никеле арсениды.Считается, что нижний предел обнаруживаемости в анализах составляет 0,1 мас.%. ОБСУЖДЕНИЕ Наличие кобальта в парараммельсбергите ирокезе не позволяет надежно оценка температуры инверсии для природных пара парараммельсбергит-раммельсбергит. Можно констатировать, что температура внедрения диарсенида никеля, безусловно, ниже 510 ° C, поскольку Парараммельсбергит могавка был экспериментально превращен в раммельсбергит на этом этапе. температура.Поскольку α-домейкит является наиболее стойкой фазой Cu-As в трещины, температуры внедрения арсенида меди не превышали 90 ° C, при низком давлении в естественной сборке. Эти решения, кроме того, очевидно, что содержание мышьяка было низким, так как богатые мышьяком фазы, такие как паксит (Cu 2 As 3 ), новакит (Cu 4 As 3 ) и (As, Cu) с.с. не были наблюдаемый. Первые два не наблюдались в исследованиях Скиннера, Адлера и Mead (1963) в системе Cu-As, что может указывать на их медленную кинетику реакции при низких температурах возможна метастабильность или их стабилизация только за счет примеси, присутствующие в анализах природных материалов, таких как Ag.С другой стороны, арсениды никеля представляют собой фазы в богатой мышьяком часть системы Ni-As. Парциальное давление мышьяка, вероятно, слишком велико. высокая, чтобы позволить образование маучерита (Ni 11 As 8 ) и Ni 5-x As 2 . Почковидная появление раммельсбергита, а также наличие древовидных трещин заполненные α-домейкитом, позволяют сделать вывод о том, что арсениды никеля были ранее размещенные в более или менее открытых полостях, в которые позже вторглись арсениды меди.Поскольку объемный состав этих «кевинавита» смеси попадают в поле Cu 3 As-NiAs 2 -NiAs, реакция на раммельсбергите контакт с растворами, богатыми медью и бедными мышьяком, приводит к образованию никколита. В некоторых случаях, когда небольшие фрагменты оказываются полностью поглощенными α-домейкитом реакция привела к полному образованию никколита, который происходит в виде небольших пузырьков в массах α-домейкита.Редкость альгодонита в сочетании с большими массами α-домейкита, фаз, которые могут сосуществовать при температурах ниже 90 ° C, указывает что жидкости содержат фракции меди и мышьяка, способствующие осаждению стехиометрическая фаза Cu 3 As.Следует отметить, что альгодонитовый пузырь в Таблица 2 (прогон d) имеет состав Cu 4.9 As, который близок к богатому мышьяком. состав альгодонита в равновесии с α-домейкитом, согласно исследования фазового равновесия Скиннер и Люс (1971), которые утверждают, что состав Cu 5.2 As. С дополнительным источник меди в прилегающих вмещающих породах, выпадение α-домейкита приведет к уменьшению содержания мышьяка в жидкостях по сравнению с содержание в них меди с последующим осаждением альгодонита и мышьяковистая медь в более поздний период.Можно возразить, что арсениды меди на самом деле были получены из действие жидкостей с исходным содержанием мышьяка на арсенид никеля и прилегающая медь в стеновых породах. Это кажется маловероятным, поскольку относительные количества арсенидов никеля, встречающиеся во время горных работ на всем полуострове Кевинау были незначительны по отношению к медным арсениды. Еще одно наблюдение, которое опровергает это возражение, – это то, что наблюдается кайма никколита между раммельсбергитом и α-домейкитом; это обод обычно очень тонкий, что указывает на ограниченную реакцию между раммельсбергитом и осаждающие жидкости α-домейкита. БЛАГОДАРНОСТИ Интерес к проблеме возник девять лет назад, когда образцы меди и Арсениды никеля были собраны лично. Стало очевидно, что Интерпретация этих парагенезисов была возможна только посредством экспериментов в синтетической системе. Этот было реализовано под руководством докторов. Г. Куллеруд и Г. Мох и использование помещений в Геофизическая лаборатория Вашингтонского института Карнеги, всем, кому я предлагаю сердечное спасибо.Доктор Б. Дж. Скиннер любезно предоставил препринт недавнего α-домейкита и исследования альгодонита перед публикацией. Финансовая помощь была оказана через Национальный научный фонд. Докторантура в 1963-1965 годах. Каталожные номера BARIAND, P., AND P. HERPIN (1960) Un arseniate de Calcium et de magnesium. Бык. Soc. Франк. Минеральная. Cristallogr. 83, 118-121. БАТЛЕР, Б.S., AND W. S. BURBANK (1929) Медные месторождения Мичигана. США. Геол. Surv. Проф. Пап . 144, 90 JOHAN Z. (1962) Paxite Cu 2 As 3 , новый арсенид меди, Acta. Univ. Carolinae Geol. 1961, 79-86,KOENIG, G A. (1960) На ироките, стибиодомейките, домейките, альгодоните и некоторые искусственные ансениды меди. амер. J. Sci. 4-я серия , 10, 439-498. РИЧАРДС, Дж.W. (1901) “Молоавкит” амер. J. Sci , 4-й Серии , 11, 457-458. СКИННЕР, Б. Дж., И. Адлер, И. К. MEAD (1963) Фазовые отношения между арсенидами меди и их применение в геологической термометрии. (abstr) Экон. Геол. 58, г. 118 ——- и Ф. Д. ЛЮС (1971) Стабильность и состав α-домейкита и альгодонита. Econ. Геол. , 66, 133-139. УИЛЬЯМ, С.А.(1963) Кристаллы раммельсбергита и альгодонита амер. Минерал . 48, 421-422. Юнд, Р. А. (1961) Фазовые соотношения в системе NiAs. Econ. Геол , д. 56, г. 127.L1295. Рукопись получена 16 декабря г.
1970; принята к печати 29 января 1971 г. | |||||||


