Металлы гальванопластика – Справочник химика 21
Практическое применение электроосаждения металлов — гальванопластика — было предложено русским акад. Б. С. Якоби в 1837 г. Свойства покрытий можно эффективно регулировать, добавляя в раствор органические вещества (Н. А. Изгарышев). Поэтому исследование влияния органических веществ на процессы электроосаждения имеет большое практическое значение. В присутствии некоторых органических веществ скорость электроосаждения ряда металлов не зависит от потенциала в области адсорбции органического вещества (М. А. Лош-карев). Наблюдаемый предельный ток оказывается меньше предельного тока диффузии. Зависимость тока от степени заполнения поверхности органическим веществом 0 описывается соотношением [c.208]Верхние и нижние скульптуры выполнены сочетанием отдельных гальванопластических деталей с деталями из листового металла. Гальванопластикой воспроизведены главным образом сложно-профилированные детали головы, руки, гирлянды и светильники остальные детали, представляющие одежду с многочисленными складками, сделаны из листовой меди и листового свинца.

Баймаков Ю. В. Электролитическое осаждение металлов. (Гальванопластика [c.264]
Важное практическое значение имеют процессы электроосаждения металлов. Впервые возможность технического применения этих процессов, а именно гальванопластика, была открыта [c.630]
Гальванотехника — один из наиболее распространенных видов электрохимического производства, который включает процессы нанесения покрытий в виде металлов и сплавов с целью защиты изделий от коррозии, защитно-декоративной отделки, повыщения сопротивления механическому износу и поверхностной твердости, сообщения антифрикционных свойств, отражательной способности (гальваностегия), а также для изготовления и размножения металлических копий (гальванопластика), [c.332]
Электрохимическое формование — гальванопластика — это метод изготовления деталей путем электроосаждения металла на форму. При этом, в отличие от гальваностегии, стремятся получить как можно менее прочное сцепление осаждаемого ме- [c. 62]
62]
В чем заключаются наиболее характерные различия в технологии электроосаждения металла в гальванопластике по сравнению с гальваностегией [c.294]
Особенно широкое распространение процессы электролиза получили в гальванопластике, открытой в 1836 г. Б. С. Якоби. Электролитическое никелирование, хромирование, меднение, серебрение, лужение (покрытие оловом) получили в настоящее время повседневное применение в народном хозяйстве. Во всех случаях покрываемое изделие служит катодом, а покрывающий металл — анодом. При этом качество покрытия зависит от состава электролитической ванны, плотности тока и пр. Если вести электролиз при малой плотности тока, то вследствие малой скорости кристаллизации металл будет отлагаться на поверхности покрываемого изделия более ровным слоем. При больших плотностях тока получается более рыхлое и дисперсное покрытие. Поэтому в зависимости от требований к качеству покрытия выбирают соответствующий режим электролиза.  267]
267]
Гальванопластикой называются процессы получения точных металлических копий с рельефных предметов электроосаждением металла. Путем гальванопластики изготовляют матрицы для прессования различных изделий, матрицы для тиснения кожи и бумаги, печатные радиотехнические схемы, типографские клише. Гальванопластику открыл Б. С. Якоби в тридцатых годах XIX века. [c.679]
ГАЛЬВАНОТЕХНИКА — осаждение металлов на поверхности металлических и неметаллических изделий при помощи электролиза. Г.— отрасль прикладной электрохимии делится на гальваностегию и гальванопластику. К гальваностегии относят процессы нанесения тонких слоев металла, прочно сцепленных с поверхностью изделий, для зашиты их от коррозии, предупреждения износа механизмов и приборов и придания изделиям красивого вида. К гальва- [c.65]
В настоящее время широкое применение находит гальванотехника-нанесение покрытий в виде металлов и сплавов (гальваностегия) и изготовление и размножение металлических копий (гальванопластика). В гальваностегии распространены электролитическое цинкование и кадмирование, лужение (т. е. покрытие оловом), свинцевание, меднение, хромирование, покрытие металлами группы железа, благородными металлами и т. п. При этом важной задачей является приготовление покрытий с заданными свойствами. Эта задача не может быть решена без знания механизма процесса электрокристаллизации металлов, что стимулирует соответствующие многочисленные исследования. Для регулирования скорости электрокристаллизации и получения осадков с заданными свойствами часто используют не простые, а комплексные электролиты и в растворы добавляют органические вещества, адсорбирующиеся на поверхности электрода.
В гальваностегии распространены электролитическое цинкование и кадмирование, лужение (т. е. покрытие оловом), свинцевание, меднение, хромирование, покрытие металлами группы железа, благородными металлами и т. п. При этом важной задачей является приготовление покрытий с заданными свойствами. Эта задача не может быть решена без знания механизма процесса электрокристаллизации металлов, что стимулирует соответствующие многочисленные исследования. Для регулирования скорости электрокристаллизации и получения осадков с заданными свойствами часто используют не простые, а комплексные электролиты и в растворы добавляют органические вещества, адсорбирующиеся на поверхности электрода.
Важным направлением электролиза водных растворов с осаждением металлов является гальванотехника. В гальванотехнике получили широкое распространение такие способы покрытия, как никелирование, хромирование, цинкование, лужение, серебрение, золочение и др. Видом гальванотехники является гальванопластика (Б. С. Якоби) — получение металлических копий различных пред-м(>тов (художественных изделий) электроосаждением металла, типографских клише, печатных схем в радиотехнике и т. д. [c.165]
С. Якоби) — получение металлических копий различных пред-м(>тов (художественных изделий) электроосаждением металла, типографских клише, печатных схем в радиотехнике и т. д. [c.165]
Гальванопластика. Электрохимическим способом можно получить точные копии металлических изделий сложной формы, например фор-камер, рефлекторов, матриц для прессования изделий, бесшовных труб, печатных схем, медалей, барельефов, скульптур и т. п. Электрохимический метод получения металлических копий изделий, открытый русским ученым Б. Якоби (1838), получил название гальванопластики. Предварительно готовят неметаллическую форму, являющуюся отпечатком оригинала. Неметаллическую форму покрывают тонким токопроводящим слоем (графитом или химически осажденной медью, никелем). Затем на форму электрохимически наносят слой меди, никеля или другого металла требуемой толщины (иногда несколько миллиметров). Заключительной операцией является отделение неметаллической формы от полученной металлической копии. При помощи одной формы можно получить большое количество копий. Гальванопластика широко применяется в радиотехнике, приборостроении, звукозаписи и других областях техники.
При помощи одной формы можно получить большое количество копий. Гальванопластика широко применяется в радиотехнике, приборостроении, звукозаписи и других областях техники.
С помощью гальванопластики изготовляют бюсты, статуи и т. д. Гальванопластика используется для нанесения сравнительно толстых металлических покрытий на другие металлы (например, образование накладного слоя никеля, серебра, золота и т. д.). [c.182]
Гальванопластика — получение путем электролиза точных, легко отделяемых металлических копий относительно значительной толщины с различных как неметаллических, так и металлических предметов, называемых матрицами. Гальванопластику используют для нанесения сравнительно толстых металлических покрытий на другие металлы (например, образование накладного слоя никеля, серебра, золота и т. д.). [c.215]
Таким образом, электролиз растворов солей с растворимым анодом сводится к окислению материала анода (его растворению) и часто сопровождается переносом металла с анода на катод.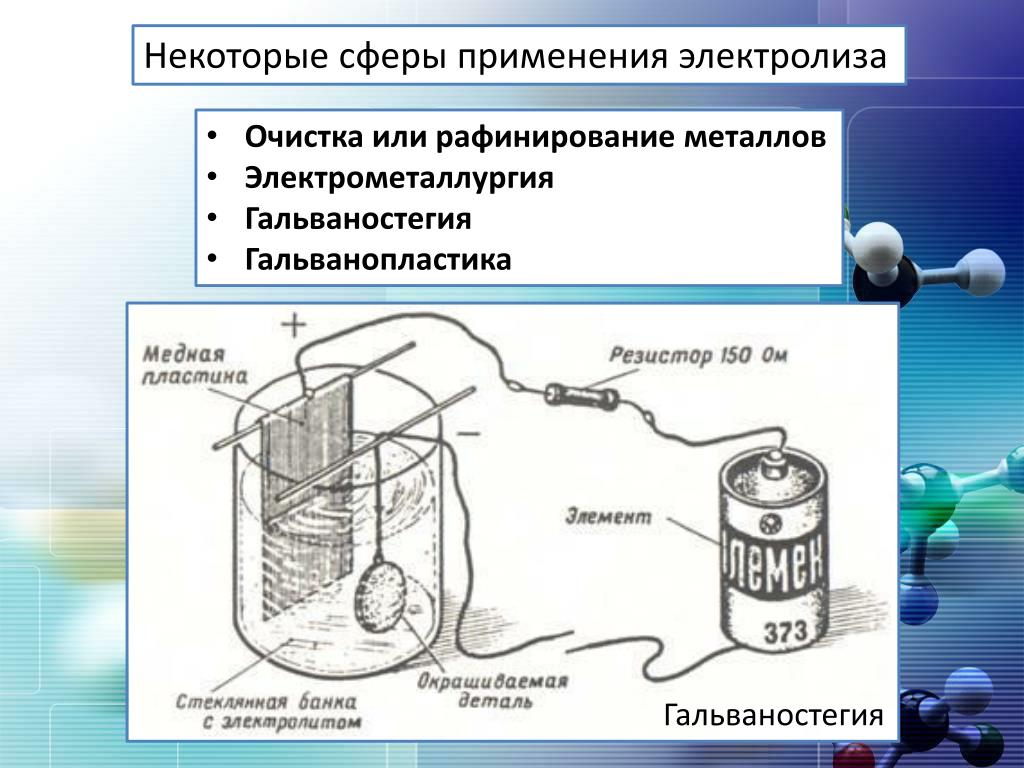
Гальванопластика применяется для нанесения довольно толстых металлических покрытий на другие металлы (образование накладного слоя меди, никеля, золота, серебра и т. д.). [c.348]
В настоящее вре мя в важнейщих отраслях промышленности многие технологические операции осуществляют с применением электрохимического метода. Получение тяжелых цветных, благородных, легких и редких металлов высокой чистоты, осуществление гальванических покрытий, обладающих особыми механическими и антикоррозионными свойствами, изыскание новых и совершенствование имеющихся химических источников тока, производство разнообразных продуктов окисления и восстановления, гальванопластика—вот далеко не полный перечень производств, использующих электрохимический метод. [c.5]
В процессе гальваностегии на поверхность металлического изделия путем электролиза наносится тонкий слой другого металла для повышения стойкости изделия к коррозии, для упрочнения его поверхности или просто для придания ему красивого внешнего вида (цинкование, хромирование, никелирование и т.
Главнейшими в настоящее время являются процессы никелирования, хромирования, цинкования, меднения, покрытия серебром, золотом и др. Наряду с этим разработаны способы осаждения некоторых редких металлов и сплавов. К гальванотехнике относится и первый промышленный электрохимический процесс воспроизведения художественных и технических рельефных предметов, получивший название гальванопластики. [c.4]
Задача гальванопластики — получение точных металлических копий путем электроосаждеиия металла. [c.213]
Выбор материала формы и изготовление ее — наиболее ответственные операции в технологии гальванопластики. Формы могут быть изготовлены из самых различных материалов — металла, пластмассы, гипса, восковых композиций, желатины и т. д. Основные требования, которые предъявляются к формам, — сохранять точный отпечаток оригинала и не взаимодействовать химически с электролитом. [c.214]
Формы могут быть изготовлены из самых различных материалов — металла, пластмассы, гипса, восковых композиций, желатины и т. д. Основные требования, которые предъявляются к формам, — сохранять точный отпечаток оригинала и не взаимодействовать химически с электролитом. [c.214]
Изготовление рефлекторов можно также осуществить средствами гальванопластики. Рефлекторы изготовляют путем осаждения металла на стеклянные формы, обработанные с высокой оптической точностью. На проводящий слой серебра, нанесенный на стеклянную форму, наращивают тонкий слой никеля, а затем медь.
Таким образом, химический эквивалент можно определить как массу вещества (г), соответствующую заряду моля электронов (F). Это соотношение будет весьма удобно для расчета электрохимических процессов (гальваностегия, гальванопластика, электрохимическая обработка металлов). [c.12]
Важнейшая область прикладной электрохимии — гальванотехника. Этим названием объединяются два направления гальваностегия — получение гальванических покрытий на металлах и гальванопластика—электрохимическое получение точных металлических копий с рельефных поверхностей (Якоби). Сейчас гальванопластика находит применение для нанесения металлических рисунков на полупроводники и непроводящие материалы (например, в производстве печатных радиосхем для миниатюрных радиоприемников). [c.214]
Этим названием объединяются два направления гальваностегия — получение гальванических покрытий на металлах и гальванопластика—электрохимическое получение точных металлических копий с рельефных поверхностей (Якоби). Сейчас гальванопластика находит применение для нанесения металлических рисунков на полупроводники и непроводящие материалы (например, в производстве печатных радиосхем для миниатюрных радиоприемников). [c.214]
Посредством электролиза осаждают металлы на поверхности рельефных изделий и, сняв затем осажденный слой металла, получают точный отпечаток рельефа. Такое копирование рельефных изделий с помощью электролиза называется гальванопластикой. Гальванопластика изобретена русским ученым С. Я. Якоби. [c.29]
В России было сделано много крупных открытий не только в области теории электрохимии, но и в приложении этой теории к практическим задачам. В 1837 г. Б, С. Якоби открыл гальванопластику — осаждение металлов на непроводящих телах. Это открытие привело к развитию многих других методов электроосаждения металлов. В России был предложен электролитический метод очистки меди. Ф. Г. Федоров (1867 г.) предложил электролитический способ изготовления медных труб без швов. Б. С. Якоби принадлежит также идея практического использования элементов в качестве источников тока. [c.8]
Это открытие привело к развитию многих других методов электроосаждения металлов. В России был предложен электролитический метод очистки меди. Ф. Г. Федоров (1867 г.) предложил электролитический способ изготовления медных труб без швов. Б. С. Якоби принадлежит также идея практического использования элементов в качестве источников тока. [c.8]
Электролиз лежит в основе гальваностегии и гальванопластики. Гальваностегия—это процесс нанесения на поверхности металлических изделий слоев других металлов. Чаще всего это делают с целью защиты от коррозии и придания изделиям красивого внешнего вида. В качестве защитных металлов наносят хром, никель н лр. Изделия, на которые наносят защитные слои, при электролизе пы-полняют функции катода. [c.245]
Применение электролиза в технике. Электролиз используют в технике в таких процессах, как гальваностегия, гальванопластика, электрохимическая обработка металлов, электромеханическая заточка и шлифование. Всем этим процессам предшествует специальная обработка поверхностей — очистка от жировых пленок (масло), оксидных слоев (травление), необходимая для дальнейших операций. При этом применяются два основных вида процессов — катодные и анод[1ые. [c.293]
Всем этим процессам предшествует специальная обработка поверхностей — очистка от жировых пленок (масло), оксидных слоев (травление), необходимая для дальнейших операций. При этом применяются два основных вида процессов — катодные и анод[1ые. [c.293]
Практическое применение электроосаждения металлов — гальванопластика — было предложено русским акад. Б. С. Якоби в 1837 г. Свойства покрытий можно эффективно регулировать, добавляя в раствор органические вещества (Н. А. Изгарышев). Поэтому исследование влияния органических веществ на процессы электроосаждеиия имеет большое практическое значение. Органические вещества действуют избирательно, тормозя восстановление одних ионов и не влияя на восстановление других. В присутствии некоторых органических веществ скорость электроосаждения ряда металлов не зависит от потенциала в области адсорбции органического вещества (М. А. Лошкарев). Наблюдаемый предельный ток оказывается меньше предельного тока диффузии. Для объяснения эффекта Лошкарева выдвинуто предположение о медленном проникновении реагирующих частиц через адсорбированный слой органического вещества. Энергия активации такого процесса вызвана необходимостью деформации пленки адсорбата при проникновении ионов к поверхности электрода. Добавление органических веществ широко используется при получении гладких и блестящих покрытий (Н. Т. Кудрявцев, К. М. Горбунова, Ю. Ю. Матулис, С. С. Кругликов и др.). Органические вещества— выравниватели и блескообразователи — адсорбируются преимущественно на выступах, где создаются более благоприятные условия для доставки этих веществ к поверхности, и препятствуют осаждению металла на этих участках, в то время как углубления постепенно заращиваются. [c.247]
Энергия активации такого процесса вызвана необходимостью деформации пленки адсорбата при проникновении ионов к поверхности электрода. Добавление органических веществ широко используется при получении гладких и блестящих покрытий (Н. Т. Кудрявцев, К. М. Горбунова, Ю. Ю. Матулис, С. С. Кругликов и др.). Органические вещества— выравниватели и блескообразователи — адсорбируются преимущественно на выступах, где создаются более благоприятные условия для доставки этих веществ к поверхности, и препятствуют осаждению металла на этих участках, в то время как углубления постепенно заращиваются. [c.247]
Первые шаги экспериментальной электрохимии были связаны с открытием Гальвани и Вольта примитивных источников тока — первых гальванических элементов. Первое практическое применеиие электрохимии металлов — гальванопластика — было предложено академиком Б. С. Якоби в 1837 г. [36]. Это открытие постепенно привело и к созданию новой отрасли техники — гальваностегии впоследствии способ гальванического покрытия получил широкое распространение, в частности, для запдиты металлов от коррозии [37, 38]. Электрохимическое осаждение металлов применяется в гидроэлектрометаллургии, например цинка [38, 39]. Сочетание анодного растворения с последующим катодным электроосаждением лежит в основе рафинирования металлов электролизом. Важнейшие способы получения таких металлов, как алюминий и магний, и некоторых редких металлов основаны на выделении их электрическим током из расплавленных электролитов [40, 41]. Электроосаждение и анодное растворение металлов применяются и в аналитической химии [42—44]. [c.32]
Электрохимическое осаждение металлов применяется в гидроэлектрометаллургии, например цинка [38, 39]. Сочетание анодного растворения с последующим катодным электроосаждением лежит в основе рафинирования металлов электролизом. Важнейшие способы получения таких металлов, как алюминий и магний, и некоторых редких металлов основаны на выделении их электрическим током из расплавленных электролитов [40, 41]. Электроосаждение и анодное растворение металлов применяются и в аналитической химии [42—44]. [c.32]
Один из трех мапжтных элементов, этот металл применяется в пятицентовых и других монетах, в гальванопластике и нихромовых сплавах. [c.165]
Гальванопластика, т. е. покрытие поверхности изделий теми или другими металлами, является первым электрохимическим и, в частности, электрометаллургическим производством. Открытие гальванопластики (1836) — заслуга Б. С. Якоби. В последующем электролитические покрытия металлами получили очень широкое распространение. Электролитическое никелирование, хромирование, лужение (покрытие оловом), кадмирование, серебрение, меднение и др. применяются для различных целей. Хромирование применяется для повышения коррозионной стойкости черных металлов, а также для увеличения твердости поверхностного слоя и сопротивления истиранию. Никелирование применяется обычно для изменения внешнего вида изделия и т. д. Все эти процессы осу-ществ 1яются методами в общем аналогичными применяемому при рафинировании мёди. Покрываемое изделие служит катодом, покрывающий металл — анодом. Качество покрытия зависит от состава электролитической ванны, плотности тока и пр. [c.447]
Электролитическое никелирование, хромирование, лужение (покрытие оловом), кадмирование, серебрение, меднение и др. применяются для различных целей. Хромирование применяется для повышения коррозионной стойкости черных металлов, а также для увеличения твердости поверхностного слоя и сопротивления истиранию. Никелирование применяется обычно для изменения внешнего вида изделия и т. д. Все эти процессы осу-ществ 1яются методами в общем аналогичными применяемому при рафинировании мёди. Покрываемое изделие служит катодом, покрывающий металл — анодом. Качество покрытия зависит от состава электролитической ванны, плотности тока и пр. [c.447]
Металлизи-рованные диэлектрики представляют большой интерес для многих отраслей промышленности, так как сочетают в себе полезные свойства металла и диэлектрика. Металлизация диэлектриков дает возможность экономить металл, снижать массу конструкций, придавать изделиям красивый внешний вид, получать пресс-формы методом гальванопластики для изготовления точного металлорежущего инструмента п копировать произведения искусства. Важное место занимает способ нанесения функциональных покрытий на диэлектрики для изделий электронной промышленности, особенно для производства печатных плат. [c.96]
Важное место занимает способ нанесения функциональных покрытий на диэлектрики для изделий электронной промышленности, особенно для производства печатных плат. [c.96]
Каковы требования к качеству сцепления электроосажденного металла с основой в гальванопластике по сравнению с гальваностегией Какие меры предпринимают для обеспечения этих требований [c.294]
К гальванотехнике относятся гальваностегия и гальванопластика. Процессы гальваностегии представляют собой нанесение путем электролиза на поверхность металлических изделий слоев других металлов для предохранения этих изделий от коррозии, для придания их поверхности твердости, а также в декоративных целях. Из многочисленных применяемых в технике Гсшьванотехнических процессов важнейшими являются хромирование, цинкование, кадмирование, никелирование, меднение и др. [c.679]
Электролиз с растворимым анодом широко применяется в технике это электролитическая очистка металлов от примесей (которые остаются в аноде), т. е. электрорафиннрование металлов, а также гальваностегия и гальванопластика, являющиеся разновидностями гальванотехники. [c.193]
е. электрорафиннрование металлов, а также гальваностегия и гальванопластика, являющиеся разновидностями гальванотехники. [c.193]
Электрохимические процессы — большая область физико-химиче-ских явлений, из которых наиболее интересны и важны возникновение разности потенциалов и получение электрической энергии за счет химической реакции (химические источники тока — ХИТ) и возникновение химических реакций за счет затраты электрической энергии (электролиз). Оба эти процесса, имеюшие обшую природу, нашли широкое применение в современной технике. Химические источники тока (гальванические элементы, аккумуляторы) используются как автономные и малогабаритные источники энергии для транспортных двигателей и машин, радиотехнических устройств и приборов управления. С помошью электролиза мы получаем различные металлы (А1 Си N1 и т. д.), обрабатываем поверхности металлических изделий, режем и полируем металл, а также создаем изделия нужной конфигурации (электрохимическая размерная обработка и гальванопластика).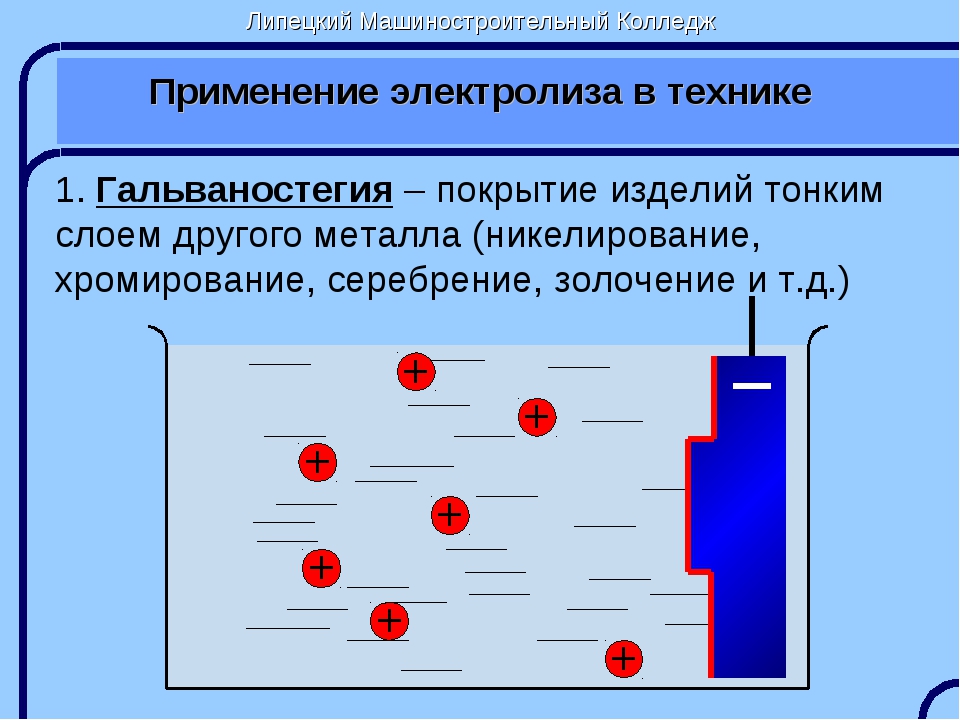 Электрохимические процессы не всегда служат на пользу человеческому обществу, иногда они приносят большой вред, вызывая процессы коррозии, ведущие к разрушению металлических конструкций и изделий. Чтобы умело бороться с нежелательными явлениями их тоже надо изучать и уметь регулировать. [c.225]
Электрохимические процессы не всегда служат на пользу человеческому обществу, иногда они приносят большой вред, вызывая процессы коррозии, ведущие к разрушению металлических конструкций и изделий. Чтобы умело бороться с нежелательными явлениями их тоже надо изучать и уметь регулировать. [c.225]
В конце ХУП1 в. и в первой половине XIX в. В. В. Петровым, Г. Деви, Т. Гротгусом, М. Фарадеем были проведены выдающиеся работы в области изучения электролиза и явлений в гальванических элементах. Русский академик Б. С. Якоби в 1836 г. осуществил практическое применение электролиза, разработал метод гальванопластики. Работы по дальнейшему изучению электродных процессов были продолжены немецким физико-химиком В. Нернстом и позже — советским ученым А. Н. Фрумкиным. Вместе со своими учениками А. Н. Фрумкин занимался изучением злектрокапилляр-ных и электрокинетических явлений. Его работы способствовали развитию теоретической и прикладной электрохимии. Выяснению причин электрохимической коррозии, ее механизма и разработке способов защиты металлов от разрушения посвящены работы советских ученых В. А. Кпстяковского, Г. В. Акимова, Н. Д. То-машова, Н. А. Изгарышева. [c.9]
А. Кпстяковского, Г. В. Акимова, Н. Д. То-машова, Н. А. Изгарышева. [c.9]
В развитии теоретической и прикладной электрохимии немалая роль принадлежит русским и советским ученым. Начало развитию электрохимии в России положили работы В. В. Петрова по электровосстановлению металлов из их окислов (1803). В 1805 г. Т Гротгус дал первое объяс-ТГениё механизма электролиза. Б. Я.коби предложил ряд конструкций химических источников тока и разработал метод гальванопластики (1837), что способствовало практическому использованию электролиза. Закономерности явления поляризации, впоследствии использованного для создания вторичных источников тока — аккумуляторов, были установлены в России Э. X. Ленцем и А. С. Савельевым (1842—1845). [c.255]
Гальванопластика служит для получения отпечатков и копий пз-делий . Например, для изготовления типографских клише или металлической копии граммофонной пластинки вначале получают их отпечатки на пластинке воска. Затем на поверхность восковой матрицы наносят порошок графитовой пыли. В результате поверхность становится проводником электрического тока. В процессе электролиза восковая матрица является катодом и на ней происходит отложение соответствующего металла в форме точной копии исх0лн010 предмета. Воск легко может быть удален с полученного предмета путем расплавления при нагревании, [c.245]
Затем на поверхность восковой матрицы наносят порошок графитовой пыли. В результате поверхность становится проводником электрического тока. В процессе электролиза восковая матрица является катодом и на ней происходит отложение соответствующего металла в форме точной копии исх0лн010 предмета. Воск легко может быть удален с полученного предмета путем расплавления при нагревании, [c.245]
Гальванопластика – Энциклопедия по машиностроению XXL
Гальванопластика нашла наиболее широкое применение в полиграфической промьппленности. Медные клише, изготовленные по этому методу, выдерживают до 260 тыс. оттисков против 25—30 тыс. [c.34]
Но зачем древним мог понадобиться гальванический элемент Вспомнили, что у античных историков упоминаются удивительные мастера, жившие во времена Клеопатры и умевшие делать золото . Но может быть, древние мастера знали гальванопластику Если соединить несколько таких элементов, то вполне можно осуществить процесс гальванического золочения, причем небольшую статуэтку при помощи такого источника тока можно покрыть тончайшим слоем золота всего за два-три часа. [c.17]
[c.17]
Электролиз применяется в электрометаллургии для получения или рафинирования цветных металлов в гальваностегии, т. е. в процессах покрытия поверхности одного металла слоем другого в гальванопластике, т е. в процессах получения электролитическим путем рельефных поверхностей. [c.356]
Синхронизирующие устройства в свободнопоршневых машинах F 01 В 11 /02 Синхронизм, устройства для индикации G 01 R 29/18 Системы [горячего водоснабжения в жилых зданиях F 24 (D 17/00, FI 9/00) сигнализации G 08 В 25/00-29/00 управления, моделирование G 06 G 7/66 центрального отопления F 24 D 1/00-12/00 электроискрового зажигания в ДВС F 02 Р 3/01 ] Сита [см. также решетки изготовление сеток для них В 21 F 27/18 использование изготовление способами гальванопластики С 25 D 1/08 из пластических материалов В 29 L 31 14 для просеивания красок В 44 D 3/10 фильтровальные В 01 D 39/(10-12) в центрифугах В 04 В 7/16] Сифонные устройства для наполнения жидкостями бутылок, банок и т. п. В 67 С 3/18 Скважины буровые (насосы для подъема жидкостей из буровых скважин F 04 (В 47/(00-14), F 1/(08, 20)) хранение в них жидкостей В 65 G 5/00, 21 F 17/16) Скиповые подъемники В 66 В (рудничные 17/(08-10) системы управления ими 1/00) Скипы В 65 (для подъема материалов D для
[c.175]
п. В 67 С 3/18 Скважины буровые (насосы для подъема жидкостей из буровых скважин F 04 (В 47/(00-14), F 1/(08, 20)) хранение в них жидкостей В 65 G 5/00, 21 F 17/16) Скиповые подъемники В 66 В (рудничные 17/(08-10) системы управления ими 1/00) Скипы В 65 (для подъема материалов D для
[c.175]
Приведем еще один пример сравнительного контроля. Отличается он от предыдущих примеров прежде всего тем, что стандартизован. Речь идет об использовании образцов шероховатости, воспроизводящих на вид и на ощупь натуральные обработанные поверхности (изготовляемых методом механической обработки, снятием позитивных отпечатков гальванопластикой или нанесением покрытий на пластмассовые отпечатки). Эти эталоны предназначены для оценки шероховатости поверхности изделия визуальным сравнением или на ощупь. Такие образцы шероховатости изготовляют в соответствии с ГОСТ 9378—75.
[c.110]
Отличается он от предыдущих примеров прежде всего тем, что стандартизован. Речь идет об использовании образцов шероховатости, воспроизводящих на вид и на ощупь натуральные обработанные поверхности (изготовляемых методом механической обработки, снятием позитивных отпечатков гальванопластикой или нанесением покрытий на пластмассовые отпечатки). Эти эталоны предназначены для оценки шероховатости поверхности изделия визуальным сравнением или на ощупь. Такие образцы шероховатости изготовляют в соответствии с ГОСТ 9378—75.
[c.110]
Для изготовления пресс-форм применяются также методы гальванопластики, металлизации и напыления. Так, гальваническое покрытие наносят на модель-эталон, изготовленный из полированного сплава на основе алюминия или цинка. В то же время при формировании плазменных покрытий на основе металлических порошков в качестве материала модели-эталона применяют металлические сплавы, графит или гипс. [c.331]
Способ изготовления пресс-форм Изготовляемые по мастер-модели (литьем, напылением, гальванопластикой) При отработке процесса, специальные случаи, художественное литье, мелкосерийное производство
[c. 358]
358]
Гальванопластика – формообразование из жидкого материала при помощи осаждения металла из раствора под действием электрического тока. [c.12]
Формообразование профилей ЭИ осуществляют несколькими методами механической обработкой, литьем, гальванопластикой, металлизацией напылением, обработкой давлением и т.д. Размеры электрода-инструмента отличаются от размеров получаемых сложных профилей деталей. [c.757]
Газы жидкие 894, 895 Гальванопластика 12 Генераторы [c.952]
Шероховатость поверхности характеризуется качественным и количественным контролем. Качественный контроль шероховатости поверхности осуществляют путем сравнения с рабочими эталонами или образцовыми деталями визуально или на ощупь. ГОСТ 9378—93 устанавливает образцы шероховатости, полученные механической обработкой, снятием позитивных отпечатков гальванопластикой или нанесением покрытий на пластмассовые отпечатки. Наборы или отдельные образцы имеют прямолинейные, дугообразные или перекрещивающиеся дугообразные расположения неровностей поверхности. На каждом образце указаны значение параметра (в мкм) и вид обработки образца. Визуально можно удовлетворительно оценить поверхности с R = 0,6,…,0,8 мкм и более. Для повышения точности используют щупы и микроскопы сравнения.
[c.378]
На каждом образце указаны значение параметра (в мкм) и вид обработки образца. Визуально можно удовлетворительно оценить поверхности с R = 0,6,…,0,8 мкм и более. Для повышения точности используют щупы и микроскопы сравнения.
[c.378]
Железо, получаемое гальванопластикой 0,21 [c.85]
Никель, получаемый гальванопластикой 0,23 [c.85]
Реплику голограммы можно сделать непосредственно с голограммы-оригинала на задубленном фоторезисте. Однако если необходимо получить очень много копий, лучше с голограммы-оригинала сделать штамп. Это выполняется методами гальванопластики, аналогичными тем, которые используются при производстве никелевых штампов для грампластинок. Никелевый штамп позволяет формовать реплики на прозрачной виниловой ленте. Температура и давление подбираются такими, чтобы можно было с уверенностью получать хорошие копии. Поскольку сырье для получения винила очень дешевое, стоимость дополнительных, копий оказывается невысокой. [c.413]
[c.413]
Электрохимическая обработка деталей основана на хорошо известных законах гальванопластики, т. е. способности анода растворяться в электролите под действием электрического тока. Одновременно с растворением металла при соответствующем составе электролита поверхность анода покрывается оксидной пленкой, прекращающей дальнейшее растворение металла в электролите. Такая пленка называется пассивной, и для продолжения процесса образовавшаяся пленка должна быть снята с анодной поверхности или разрушена. Различают два способа ликвидации пленки — электрохимический и анодно-механический. При электрохимическом способе обработки металла пассивная оксидная пленка удаляется силами электрического поля, а при анодно-механическом — механическим путем. [c.62]
Гальванический сплав Ag—Си получил применение в технике в качестве контактного покрытия, в гальванопластике и в качестве подслоя под эмаль.
 Компактные осадки Ag—Си получаются из цианистого электролита лишь при большой концентрации металлов в растворе. Для получения сплава, содержащего 5—8% Си, рекомендуется следующий состав электролита (в Г/л)
[c.286]
Компактные осадки Ag—Си получаются из цианистого электролита лишь при большой концентрации металлов в растворе. Для получения сплава, содержащего 5—8% Си, рекомендуется следующий состав электролита (в Г/л)
[c.286]Материал и метод изготовления ЭИ (механическая обработка, гальванопластика, металлизация напылением, штамповка, прессование) след ет выбирать в зависимости от вида электроэрозионной операции, материала детали, режимов, площади обработки, сложности формы обрабатываемой поверхности, ее точности, шероховатости, а также программы выпуска деталей. [c.839]
Гальванотехника — нанесение металлических покрытий на поверхность изделий методом электроосаждения. Катодом служит покрываемое изделие. Гальванотехника включает гальваностегию (нанесение тонких покрытий, прочно сцепленных с покрываемым металлом) я гальванопластику — получение сравнительно толстых, легко отделяющихся слоев). Гальванопластика позволяет получать точные копии с различных предметов. [c.111]
[c.111]
Каково назначение гальваностегии и гальванопластики [c.124]
Начальный период развития отечественной электротехнической промышленности был связан с практическим применением электрической энергии для целей связи, электрической сигнализации, гальванопластики и изготовления химических источнит ов электрического тока. [c.91]
Гальванопластика нашла наиболее широкое применение в полиграфической промышленности. Медные клише, изготов-шные по этому методу, выдерживают до 250 тыс. оттисков ютив 25—30 тыс. оттисков, которые можно получить на цин-эвых клише, сделанных глубоким травлением. [c.19]
Кроме этого, можно применять фтороборатные растворы и сульфатные (главным образом, в гальванопластике). Во всех растворах при нанесении медного покрытия используются медные аноды. [c.95]
Явления, происходящие на катоде — восстановление и выделение металла, — используются в основном в гальванопластике и гальваностегии. Они же лежат в основе операции катодного снятия окалин и электроцементации.
[c.947]
Они же лежат в основе операции катодного снятия окалин и электроцементации.
[c.947]
Трубы F” 16 L прокладка (1/00-1/04 сквозь стены или перегородки 5/00-5/02) ремонт 55/10-55/18 телескопические 27/12 теплоизоляция 59/(14-16) укладка 1/00-1/04 шарнирные соединения 27/02-06) грузозахватные устройства для их подъема В 66 С 1/56 защитные для прокладки кабелей и проводов в зданиях или на транспортных средствах Н 02 G 3/04 испытание на герметичность G 01 М 3/08, 3/38 канализационные сливные, устранение засорений G 03 С 1, 30-1/308 керамические котлов G распыливающие для оросительных холодильников F 25/06) крепление гибка 7/00-7/16, 9/00-9/18 гофрирование 15/(00-12) изменение диаметра концов труб 41/00 образование пазов в них 17/(00-04) изготовление фланцев 19/00 перфорирование 28/28 правка 3/00-3/16 расширители для них при обработке давлением 39/(08-20) соединение способами обработки давлением 39/04 фальцовка 39/02 отбортовка кромок труб 19/00) В 21 D изготовление способами обработки металла без снятия стружки С 37/(06-30) зкструдирование. м С 37/(06-30)) литьем в формах, вращающихся вокруг своей оси, В 22 D 13/02 способами гальванопластики С 25 D 1/02) обработка резцами В 23 D 79/12 очистка (В 08 В 9/02 химическими средствами С 23 G 3/04) покрытие металлами электрическим способом или способом электрофореза С 25 D 7/04,
[c.196]
м С 37/(06-30)) литьем в формах, вращающихся вокруг своей оси, В 22 D 13/02 способами гальванопластики С 25 D 1/02) обработка резцами В 23 D 79/12 очистка (В 08 В 9/02 химическими средствами С 23 G 3/04) покрытие металлами электрическим способом или способом электрофореза С 25 D 7/04,
[c.196]
Фитинги изготовление ковкой или штамповкой В 21 К 1/14 F 16 маслопроводов N 21/00 пластмассовые L 47/(00—06) предотвращение коррозии L 58/00) ручные инструменты для вставки в шланги В 25 В 27/10> Фланцы [инструменты для сборки В 25 В 27/16 В 21 ковка К 23/04 отгибание фланцев металлических частей D 19/00) соединения труб (путем загибания фланцев F 16 L 13/14 фланцевые (в теплообменных аппаратах F 28 F 9/12 и шлангов F 16 L 23/(00—04))>] Флоккуляция очистке воды и сточных вод С 02 F 1/52-1/56) как способ нанесения жидкостей на поверхность В 05 D 1/14, 1/16> Флотация очистки воды и сточных вод С 02 F 1 /24 для разделения руд В 03 В 5/28-5/46 для транспортирования сыпучих материалов по желобам и трубам В 65 G 53/00)) Флюсы, использование выращивания монокристаллов С 30 В 9/12 для нанесения защитного слоя на изделия С 23 С 2/30 С 21 (для обработки расплавленных ферросплавов С 7/076 при получении чугуна В 3/02) (при рафинировании С 22 В 9/10 при сварке и резке В 23 К 35/(36 -368)) металлов) Фольга (изгопювлеиие (В 21 D 33/00 способами гальванопластики С 25 D 1/04 для упаковки В 65 В 9/00) В 65 Н намотка 18/00 подача, намотка, размотка, укладка и т. п.) обработка В 41 N 1/00, 1/14 прокатка В 21 В 1/40) Фонари (как осветительные устройства) поездные для сигнализации В 61 L 15/02 F 21 уличные S 1/10 шахтерские L 11/00) в устройствах для зажига1шя F 23 Q 13/04 кабин самолетов В 64 С 1/14) Форкамеры F 02 (в воздушно-реактивных двигателях К 1104-7двигателей внутреннего сгорания В 19/(00—18)) Форматные пилы В 27 В 5/06
[c.203]
п.) обработка В 41 N 1/00, 1/14 прокатка В 21 В 1/40) Фонари (как осветительные устройства) поездные для сигнализации В 61 L 15/02 F 21 уличные S 1/10 шахтерские L 11/00) в устройствах для зажига1шя F 23 Q 13/04 кабин самолетов В 64 С 1/14) Форкамеры F 02 (в воздушно-реактивных двигателях К 1104-7двигателей внутреннего сгорания В 19/(00—18)) Форматные пилы В 27 В 5/06
[c.203]
Изготовление таких инструментов возможно различными способами по обычной абразивной техвологии с введением проводящих добавок в состав массы круга методами гальванопластики —закреплением зерен абразива гальванически формирующимся металлом, засыпкой абразива в расплавленный металл и отливкой массы в форму прессованием абразивных смесей на металлических связках и т. д. [c.71]
В 1985—1986 гг. в Резенде (Бразилия) проведены испытания первого каскада опытного завода, состоящего из 24 ступеней с радиусом отклоняющей канавки 100 мкм.
 Построены и испытаны в ФРГ разделительные ступени трех типоразмеров ( R-33, R-100, R-300) с компрессорами производительностью 33, 100 и 300 тыс. м /ч соответственно. В качестве газа-разбавителя принят гелий. Разделительная мощность R-300 с использованием разделительных элементов, изготовленных методом рентгеновской литографии и гальванопластики (LlGA-метод), составит 15—22 тыс. ЕРР/год, т. е. в 1,5—2 раза больше мощности самой крупной диффузионной ступени на заводе фирмы Евродиф .
[c.233]
Построены и испытаны в ФРГ разделительные ступени трех типоразмеров ( R-33, R-100, R-300) с компрессорами производительностью 33, 100 и 300 тыс. м /ч соответственно. В качестве газа-разбавителя принят гелий. Разделительная мощность R-300 с использованием разделительных элементов, изготовленных методом рентгеновской литографии и гальванопластики (LlGA-метод), составит 15—22 тыс. ЕРР/год, т. е. в 1,5—2 раза больше мощности самой крупной диффузионной ступени на заводе фирмы Евродиф .
[c.233]Более 75% молибдена применяют для легирования сталей, используемых в авиа- и автомобилестроении, при изготовлении лопаток турбин и др. Весьма перспективны жаропрочные (для реактивных двигателей) и кислотоупорные (аппараты химической промышшенности) сплавы так, сплав Fe — Ni — Мо стоек по отношению ко всем кислотам (кроме Hf) до 100°С. Молибден — важнейший конструкционный материал в производстве нитей для электрических ламп и катодов для электровакуумных приборов. Его используют в гальванопластике (молибденирова-ниё), а также в аналитической химии для определения фосфора, мышьяка, кремния, германия и некоторых других элементов.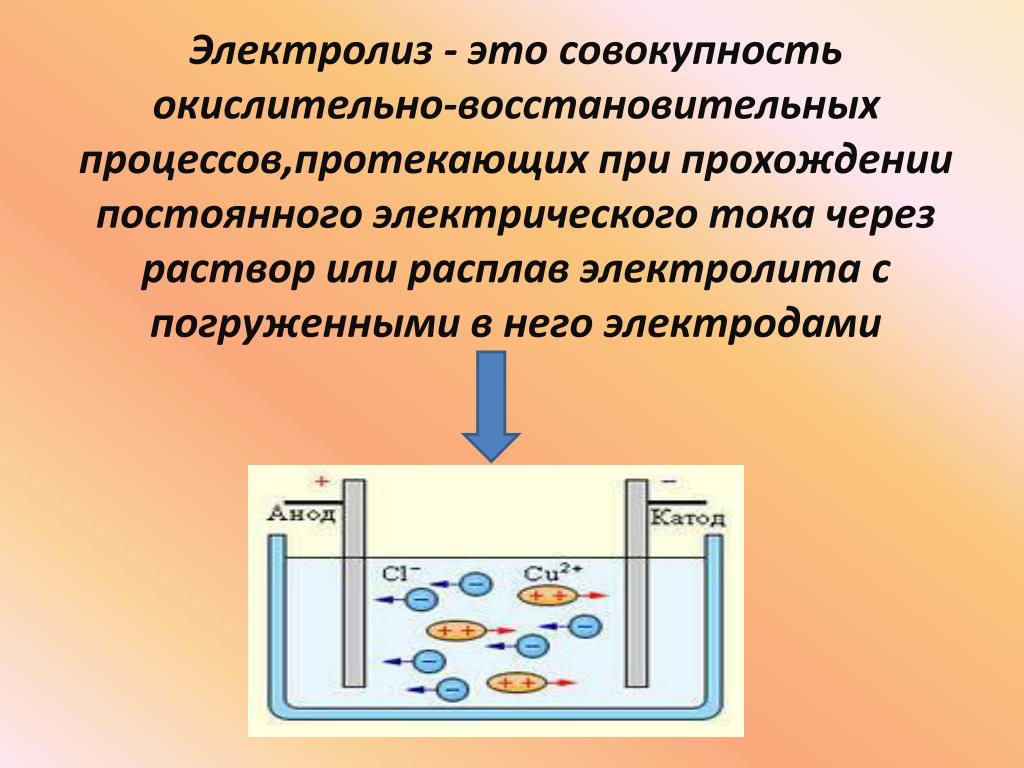 [c.199]
[c.199]
Материал и метод изготовления ЭИ (механическая обработка, гальванопластика, элек- [c.731]
Одна из первых попыток ввести общую для всех единицу сопротивления проводников электрическому току принадлежит русскому изобретателю гальванопластики, электродвигателя, пишущего телеграфа и гальванических мин Б.С. Якоби (1801-1874 гг.). Единица сопротивления Якоби быда определена как сопротивление медной проволоки длиной 6,358 фута (1 фут = 30,5 см) и диаметром 0,00336 дюйма (1 дюйм = 2,54 см). [c.34]
Получаемые гальванопластикой никелевые формы, которые используются уже более 15 лет, в результате последних усовершенствований представляют собой плотную конструкцию без пор, с хорошо отполированной формующей и гладкой задней поверхностями. Стоимость таких форм снизилась, и разработаны методы изготовления форм со сложной конфигурацией. Фирма Груммэн эароспейс применяет никелевые формы, получаемые гальванопластикой, для формования деталей самолетов. Температурный коэффициент линейного расширения никеля того же порядка, что и у стеклопластиков.
[c.86]
Температурный коэффициент линейного расширения никеля того же порядка, что и у стеклопластиков.
[c.86]
Прозрачные лаки применяют в гальванопластике для предупреждения осаждения металла на некоторых частях изделий прп погружении их в гальваническую ванну. Эти лаки часто называют защитными (Stop-off). Наряду с хорошей адгезией они должны обладать стойкостью к действию растворов различных электролитов. Состав такого лака на основе полиакрилата приводится в рецептуре 69. [c.497]
Электрод-инструмент для ЭХО изготовляют из сплавов с хорошей электрической проводимостью и высокой стойкостью против коррозии меди, латуни, бронзы, коррозионно-стойких сталей, жаропрочных и титановых сплавов, графита и др.). Электроды из коррозионно-стойких сталей применяют для изготовления лопаток турбин и компрессоров, а также штампов и пресс-форм. Из титановых сплавов изготовляют тонкие трубчатые электроды для прошивания глубоких отверстий. Графит применяют в условиях единичного и. мелкосерийного производства деталей, а также при обработке вращающимся электродом-диском. Формообразование профилей ЭИ осуществляют несколькими методами механической обработкой, литьем, гальванопластикой, металлизацией напьшением, вихревым копированием, обработкой давлением и т. д. Размеры электрода-инструмента отличаются от раз.меров получаемых сложных профилей деталей.
[c.866]
мелкосерийного производства деталей, а также при обработке вращающимся электродом-диском. Формообразование профилей ЭИ осуществляют несколькими методами механической обработкой, литьем, гальванопластикой, металлизацией напьшением, вихревым копированием, обработкой давлением и т. д. Размеры электрода-инструмента отличаются от раз.меров получаемых сложных профилей деталей.
[c.866]
Reaktiv – Темы проектов
Примерные темы рефератов (докладов), индивидуальных проектов
• Биотехнология и генная инженерия — технологии XXI века.
• Нанотехнология как приоритетное направление развития науки и производства в Российской Федерации.
• Современные методы обеззараживания воды.
• Аллотропия металлов.
• Жизнь и деятельность Д. И. Менделеева.
• «Периодическому закону будущее не грозит разрушением…»
• Синтез 114-го элемента — триумф российских физиков-ядерщиков.
• Изотопы водорода.
• Использование радиоактивных изотопов в технических целях.
• Рентгеновское излучение и его использование в технике и медицине.
• Плазма — четвертое состояние вещества. • Аморфные вещества в природе, технике, быту.
• Охрана окружающей среды от химического загрязнения. Количественные характеристики загрязнения окружающей среды.
• Применение твердого и газообразного оксида углерода (IV).
• Защита озонового экрана от химического загрязнения.
• Грубодисперсные системы, их классификация и использование в профессиональной деятельности.
• Косметические гели.
• Применение суспензий и эмульсий в строительстве.
• Минералы и горные породы как основа литосферы.
• Растворы вокруг нас. Типы растворов.
• Вода как реагент и среда для химического процесса.
• Жизнь и деятельность С. Аррениуса.
• Вклад отечественных ученых в развитие теории электролитической диссоциации.
• Устранение жесткости воды на промышленных предприятиях.
• Серная кислота — «хлеб химической промышленности».
• Использование минеральных кислот на предприятиях различного профиля.
• Оксиды и соли как строительные материалы.
• История гипса.
• Поваренная соль как химическое сырье.
• Многоликий карбонат кальция: в природе, в промышленности, в быту.
• Реакции горения на производстве и в быту.
• Виртуальное моделирование химических процессов.
• Электролиз растворов электролитов.
• Электролиз расплавов электролитов.
• Практическое применение электролиза: рафинирование, гальванопластика, гальваностегия.
• История получения и производства алюминия.
• Электролитическое получение и рафинирование меди.
• Жизнь и деятельность Г. Дэви.
• Роль металлов в истории человеческой цивилизации. История отечественной черной металлургии. Современное металлургическое производство.
• История отечественной цветной металлургии. Роль металлов и сплавов в научно- техническом прогрессе.
• Коррозия металлов и способы защиты от коррозии.
• Инертные или благородные газы.
• Рождающие соли — галогены.
• История шведской спички.
• История возникновения и развития органической химии.
• Жизнь и деятельность А. М. Бутлерова.
• Витализм и его крах.
• Роль отечественных ученых в становлении и развитии мировой органической химии.
• Современные представления о теории химического строения.
• Экологические аспекты использования углеводородного сырья.
• Экономические аспекты международного сотрудничества по использованию углеводородного сырья.
• История открытия и разработки газовых и нефтяных месторождений в Российской Федерации.
• Химия углеводородного сырья и моя будущая профессия.
• Углеводородное топливо, его виды и назначение.
• Синтетические каучуки: история, многообразие и перспективы.
• Резинотехническое производство и его роль в научно-техническом прогрессе.
• Сварочное производство и роль химии углеводородов в нем.
• Нефть и ее транспортировка как основа взаимовыгодного международного сотрудничества.
Фото с сайта https://pixabay.com/ru
Применения электролиза – гальваника, гальванопластика
Электролит: вещество, часто ионопроводящий полимер, который содержит свободные ионы в электролите, по которому течет электрический ток. Если ионы, как в большинстве твердых солей, неподвижны, электролиз будет невозможен.
Электропитание постоянного тока (DC): обеспечивает энергию, необходимую для генерации или разряда ионов электролита. Электрический ток переносится во внешней цепи электронами.
Два электрода: это электрические проводники, обеспечивающие физический интерфейс между электролитом и электрической цепью, обеспечивающей электроэнергию.
1. Добыча металла (электрометаллургия)
Электрометаллургия – это процесс электролиза для извлечения металла из руды. Электролиты из расплавленных электролитов позволяют получать такие металлы, как натрий, калий, магний, кальций, алюминий и т. Д. Существует два метода извлечения металлов в зависимости от физического состояния руды.В первом способе руду обрабатывают сильной кислотой для получения соли, и такой раствор соли подвергают электролизу для высвобождения металла. Во втором процессе руда находится в расплавленном состоянии и подвергается электролизу в печи.
Электролиты из расплавленных электролитов позволяют получать такие металлы, как натрий, калий, магний, кальций, алюминий и т. Д. Существует два метода извлечения металлов в зависимости от физического состояния руды.В первом способе руду обрабатывают сильной кислотой для получения соли, и такой раствор соли подвергают электролизу для высвобождения металла. Во втором процессе руда находится в расплавленном состоянии и подвергается электролизу в печи.
(i) Добыча цинка:
Серная кислота используется для обработки цинковой руды. Во время процесса электролиза, участвующего в этой реакции, в результате получается раствор сульфата цинка, который также действует как электролит для электролитической реакции. Катоды в резервуаре с электролитом сделаны из алюминия, а аноды – из свинца.Плотность тока поддерживается на уровне 1000 А / м², а на катоде осаждается цинк. Потребление энергии составляет от 3000 до 5000 кВт / ч на тонну.
(ii) Добыча алюминия:
Бокситы и криолит – это алюминиевые руды. Они химически обрабатываются и восстанавливаются до оксида алюминия, затем растворяются в плавленом криолите и подвергаются электролизу в печи. На дне оседают отложения алюминия. Температура печи составляет около 1000 ° C, чтобы электролит оставался в расплавленном состоянии. Для завершения процесса требуется ток около 4000 ампер, а потребляемая энергия составляет от 20 000 до 25 000 кВтч на тонну.
Они химически обрабатываются и восстанавливаются до оксида алюминия, затем растворяются в плавленом криолите и подвергаются электролизу в печи. На дне оседают отложения алюминия. Температура печи составляет около 1000 ° C, чтобы электролит оставался в расплавленном состоянии. Для завершения процесса требуется ток около 4000 ампер, а потребляемая энергия составляет от 20 000 до 25 000 кВтч на тонну.
2. Производство неметаллов
Электролиз используется для получения неметаллов, таких как водород, фтор, хлор. Водород получают в присутствии электролитов, таких как H₂SO₄ и KNO₃, путем электролиза воды.
3. Рафинирование металлов
Основные преимущества электролитических процессов извлечения металла заключаются в том, что чистота получаемого продукта составляет от 98 до 99%. Электролиз используется для дальнейшей очистки. Анод изготовлен из извлеченного металла.Катод осаждает чистый металл. Электролит состоит из металлического раствора, такого как медь, сульфат меди и никель, хлорид никеля. Энергозатратность электролитического процесса при рафинировании меди составляет от 150 до 300 кВтч / т рафинированной меди. Чистоту меди можно повысить за счет электрорафинирования. В этом случае используется тот же принцип гальваники или электроосаждения. Электролит представляет собой раствор ионов меди, например сульфата меди. Катод представляет собой полоску чистой меди, а анод – грязный кусок меди.На аноде: атомы меди растворяются, образуя ионы меди из нечистой меди. Это приводит к уменьшению размера анода. Примеси собираются в ячейке и отваливаются от анода. На катоде: ионы Cu2 + мигрируют к катоду, где они осаждаются в виде твердой меди на катоде. Катод становится толще (увеличивается в размерах).
Энергозатратность электролитического процесса при рафинировании меди составляет от 150 до 300 кВтч / т рафинированной меди. Чистоту меди можно повысить за счет электрорафинирования. В этом случае используется тот же принцип гальваники или электроосаждения. Электролит представляет собой раствор ионов меди, например сульфата меди. Катод представляет собой полоску чистой меди, а анод – грязный кусок меди.На аноде: атомы меди растворяются, образуя ионы меди из нечистой меди. Это приводит к уменьшению размера анода. Примеси собираются в ячейке и отваливаются от анода. На катоде: ионы Cu2 + мигрируют к катоду, где они осаждаются в виде твердой меди на катоде. Катод становится толще (увеличивается в размерах).
4. Производство химикатов
Многие химические вещества, такие как каустическая сода (NaOH), хлор и т. Д., Производятся в больших масштабах посредством электролиза.При крупномасштабном электролизе также производятся перманганат калия, водород, кислород и т. Д.
Д.
5. Гальваника
Гальваника – это покрытие объекта тонкой металлической пленкой, осаждаемой во время электролиза раствором электролита. Гальваника часто используется на таких предметах, как ножи и вилки (серебряная пластина), чтобы получить привлекательную и долговечную отделку. Он также используется для защиты металлов, подверженных коррозии. Например, относительно инертный металлический кадмий часто наносят на стальные детали для предотвращения коррозии.Гальваника – очень ценный промышленный процесс, но его использование требует дорогостоящей и постоянно эффективной обработки образующихся отходов. Возможно изготовление недорогих посеребренных украшений методом гальваники. Золотые кольца, от которых пальцы становятся зелеными, на самом деле представляют собой медные кольца с гальваническим покрытием из золота.
Изделие, на которое наносится покрытие, используется в качестве катода в процессе гальваники, а металл, нанесенный на изделие, используется в качестве анода. Электролитический раствор или «ванна» содержит металлическую соль металла.Низковольтный электрический ток заставляет ионы металлов из ванны получать электроны от катода и оседать на катоде (объекте) в виде металлического покрытия. Это также приводит к тому, что атомы металла теряют электроны на аноде и уходят в ванну в виде ионов. Анод постепенно исчезает по мере нанесения покрытия и поддерживает концентрацию иона металла в ванне. Многие токсичные растворы используются в гальванических операциях. Предметы, покрываемые концентрированными кислотными или щелочными растворами, тщательно очищаются от жира и грязи.В конечном итоге из-за загрязнения чистящие растворы становятся неэффективными, и их необходимо утилизировать.
Электролитический раствор или «ванна» содержит металлическую соль металла.Низковольтный электрический ток заставляет ионы металлов из ванны получать электроны от катода и оседать на катоде (объекте) в виде металлического покрытия. Это также приводит к тому, что атомы металла теряют электроны на аноде и уходят в ванну в виде ионов. Анод постепенно исчезает по мере нанесения покрытия и поддерживает концентрацию иона металла в ванне. Многие токсичные растворы используются в гальванических операциях. Предметы, покрываемые концентрированными кислотными или щелочными растворами, тщательно очищаются от жира и грязи.В конечном итоге из-за загрязнения чистящие растворы становятся неэффективными, и их необходимо утилизировать.
На качество металлического покрытия, образованного гальваническим способом, влияет ряд факторов:
Концентрация катионов, подлежащих уменьшению, тщательно контролируется в растворе для нанесения покрытий.
 Необходимо избегать нежелательных побочных реакций.
Необходимо избегать нежелательных побочных реакций.Следует тщательно учитывать тип и концентрацию электролита.
В раствор должны быть включены соединения для контроля кислотности и повышения проводимости.
Некоторые составы делают его более ярким или гладким, чтобы покрыть металл.
Анод должен иметь форму катодного объекта во многих гальванических ячейках для получения равномерного металлического покрытия.
6. Электротипирование
Это процесс, с помощью которого процесс гальваники воспроизводит пропилы дерева и т. Д. В меди. В этом процессе сначала изготавливают форму из воска, затем покрывают черным свинцом, чтобы придать ей металлическую поверхность, а затем подвергают процессу электроосаждения.Таким образом, на подготовленной поверхности образуется медная пленка.
7. Электроформование
Это еще одно приложение для электроосаждения. Воспроизведение объектов электроосаждением на какой-либо форме или форме известно как электроформование. Это еще один полезный пример среди многих приложений электролиза. Сначала мы должны получить отпечаток предметов на воске или другом воскообразном материале. Чтобы сделать его проводящим, поверхность восковой формы, которая имеет точный слепок объекта, покрывается графитовым порошком.Затем форма погружается в качестве катода в раствор электролита. Металлический электролит будет осаждаться на вдавленной графитовой поверхности формы во время процесса электролиза. Изделие будет удалено после получения слоя желаемой толщины, и воск будет расплавлен, чтобы получить воспроизведенный объект в виде металлической оболочки. Воспроизведение диска с граммофонной пластинкой – популярное применение гальванопластики. Оригинальная запись происходит на пластинке восковой композиции. Затем эта восковая форма покрывается золотым порошком, чтобы сделать ее проводящей.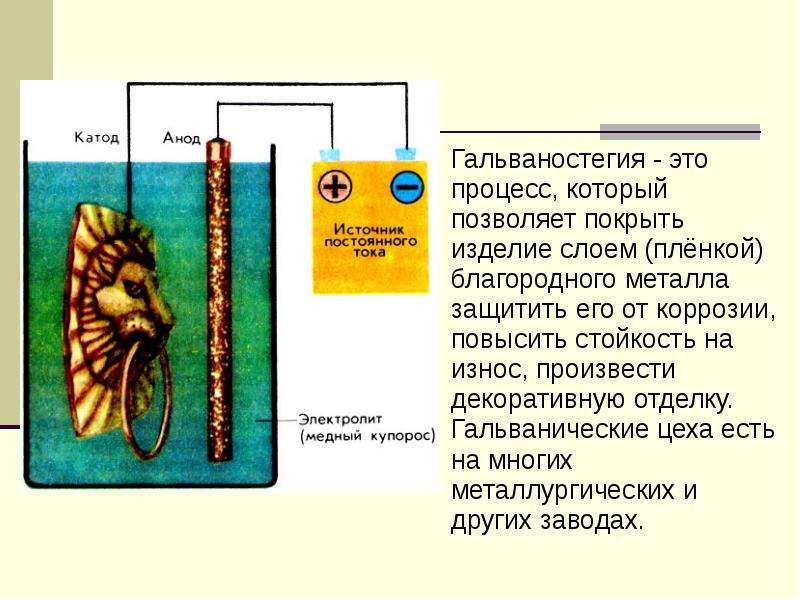 Эта форма затем погружается в качестве катода в электролит медного купороса. Использование медного анода обеспечивает насыщение раствора. На восковой форме гальваническое формование меди позволяет получить шаблон, который используется для штамповки большого количества дисков шеллака.
Эта форма затем погружается в качестве катода в электролит медного купороса. Использование медного анода обеспечивает насыщение раствора. На восковой форме гальваническое формование меди позволяет получить шаблон, который используется для штамповки большого количества дисков шеллака.
8. Электроочистка
Предметом, подлежащим очистке от масел и жиров, является катод, и раствор пропускается через резервуар для железа или чан, заполненный раствором электролита и сильным током. На катоде образуется едкий натр и водород, удаляющий жир с поверхности изделия.Этот процесс известен как катодная очистка и применяется к цинку и алюминию. Изделие изготовлено анодным для анодной очистки.
9. Определение эквивалентных масс элементов
Количество металлов, осажденных на катодах двух элементов, пропорционально их эквивалентным массам соответствующих металлов, согласно второму закону электролиза, когда одинаковое количество электронного тока прошли через солевые растворы двух разных клеток. Если количество металлов, нанесенных на катоды, равно WA и WB, то
Если количество металлов, нанесенных на катоды, равно WA и WB, то
\ [\ frac {W_ {A}} {W_ {B}} = \ frac {Equivalent \: Mass \: of \: A} {Equivalent \: Масса \: of \: B} \]
Зная эквивалентную массу одного металла, можно вычислить эквивалентную массу другого металла из приведенного выше соотношения.Этот метод также может определять эквивалентные массы тех неметаллов, которые выделяются на анодах.
10. Толщина любого слоя покрытия
Метод электролиза также можно использовать для расчета толщины покрытого слоя любого материала. Для этого нам просто нужно знать размеры материала с покрытием, и мы получим его толщину.
Каковы применения электролиза
Каковы применения электролиза Применение электролизаПроцесс электролиза имеет много важных промышленных применений.Вот некоторые из них:
- Электролиз используется в промышленности для производства многих металлов и неметаллов (например, алюминия, магния, хлора и фтора).
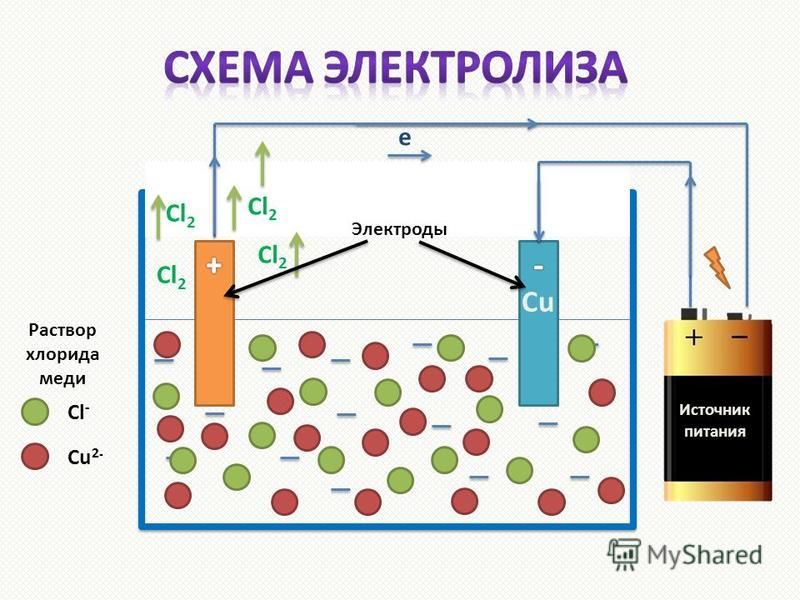
- Электролиз обычно используется для покрытия одного металла другим. Метод покрытия одного металла другим с помощью электрического тока называется гальваникой. Общая установка, используемая для нанесения гальванического покрытия на объект, показана на рисунке.
При нанесении гальванических покрытий используется следующий метод:- Покрываемый объект выполнен в виде катода.
- Металл, наносимый на объект, принимают в виде электрода и делают его анодом.
- Электролит содержит растворенные соли металла, на который наносится покрытие.
- Ионы металла (которые заряжены положительно) притягиваются катодом и, следовательно, движутся к объекту и осаждаются на нем.
Гальваника используется для многих целей. Вот несколько примеров.
- Металлы, которые легко подвержены коррозии, защищены покрытием из металла, который не подвержен коррозии.Никель и хром широко используются в автомобильной промышленности для нанесения покрытий.

- Для украшения используется гальваника. Например, столовые приборы, статуи и украшения из более дешевых металлов покрываются дорогими металлами, такими как золото и серебро, чтобы улучшить их внешний вид.
- Гальваника используется при производстве печатных плат (небольшие схемы с компонентами, обычно напечатанными на пластиковой плате), которые используются в телевизорах, компьютерах и т. Д.
Деятельность
Цель: Наблюдать за гальваническим покрытием меди на нержавеющей стали.
Необходимые материалы: 20 г сульфата меди, растворенного в 100 мл воды, медная полоска или медный стержень, два провода, батарея (3-5 вольт), химический стакан и объект, подлежащий гальванике (ложка из нержавеющей стали или монета). .
Метод:
1. Возьмите раствор медного купороса в стакан.
2. Подключите медную полоску (действует как анод) к положительной клемме аккумулятора с помощью соединительного провода.
3. Аналогичным образом подключите объект, на который будет нанесено гальваническое покрытие (действует как катод), к отрицательной клемме батареи с помощью соединительного провода.
4. Окуните медную полоску и объект, на который нужно наносить гальваническое покрытие, в раствор сульфата меди.
5. Гальванировать 20-25 минут или до образования однородного коричневого налета металлической меди на объекте.
Электролиз используется при рафинировании нечистых металлов. Этот метод, называемый электрорафинированием, можно использовать для очистки металлов, таких как медь, золото и серебро. Вот как проводится очистка меди.
Деятельность
Цель: Наблюдать за осаждением меди с использованием медных электродов и раствора сульфата меди
Необходимые материалы: Аккумулятор, электрические провода, толстая медная полоса, тонкий медный провод (со снятой оболочкой), медь сульфатный раствор и стеклянный стакан.Стеклянный стакан следует выбросить после эксперимента.
Метод: Проведите эксперимент, как показано на рисунке. Подождите некоторое время и посмотрите, что произойдет с катодом.
Наблюдение: Вы увидите, что катод из чистой меди покрывается медным покрытием.
Электротехника – что такое практическое применение электролиза
Практическое применение электролиза
Явление электролиза имеет множество промышленных и коммерческих применений.Некоторые из них обсуждаются ниже в качестве иллюстрации.
(1) Гальваника. Процесс нанесения тонкого слоя металла высшего качества (например, золота, серебра, никеля и т. Д.) На металл более низкого качества (например, железо) известен как гальваника. Гальваника предназначена для обеспечения хорошего внешнего вида и защиты объекта от коррозии. На рис. (А) показано простое расположение серебряного покрытия. Покрываемый объект (например, небольшой железный ключ) используется в качестве катода. Наплавленный металл (в данном случае серебро) становится анодом.В качестве электролита в данном случае используется раствор соединения осаждаемого металла AgNO 3 . Когда d.c. При подаче питания на электроды серебряный стержень (то есть анод) непрерывно растворяется в растворе и осаждается на катоде (то есть на объекте).
(а) (б)
рисунок
(2) Рафинирование металлов .Многие металлы очищаются в процессе электролиза. Загрязненный металл используется в качестве анода, а небольшой кусок чистого металла используется в качестве катода. В качестве электролита используется солевой раствор очищаемого металла. Рис. (B) показывает простую установку для электролитического рафинирования * меди. Когда d.c. подается на электроды, чистая медь с анода переходит в раствор и осаждается на катоде. Примеси оседают на дно контейнера и образуются «анодным шламом».Точно так же электролитический процесс можно использовать для рафинирования других металлов, таких как серебро, золото, платина и никель.
(3) Производство химикатов. Процесс электролиза широко используется для промышленного производства таких химикатов, как карбонат натрия, бикарбонат натрия, каустическая сода и т. Д.
(4) Извлечение металлов из руд . Многие металлы, такие как Al, Mg, Zn, Cu и т. Д., Извлекаются из руд путем электролиза с образованием кислорода и водорода.Путем электролиза кислой воды можно получить кислород и водород.
(5) Конденсатор электролитический . Электролитический конденсатор состоит из двух алюминиевых фольг, в которых в процессе электролиза зажат очень тонкий диэлектрик. Две алюминиевые фольги (которые действуют как электроды) погружаются в раствор борной кислоты, глицерина и аммиачной воды. Когда ток проходит между анодом и катодом, на поверхности анода образуется очень тонкая пленка оксида алюминия (Al 2 0 3 ).Эта оксидная пленка действует как диэлектрик. Поскольку оксидная пленка очень тонкая, электролитический конденсатор имеет очень большую емкость.
(6) Анодирование . Это процесс нанесения оксида алюминия на сам алюминий путем электролиза для защиты от коррозии. Алюминиевое изделие выполнено анодным и расширенным. H 2 SO 4 – электролит.
(7) Электропечать . Это процесс, при котором мы получаем впечатление страницы книги из ** меди.Обычный шрифт предназначен для формирования страницы книги. Затем его поливают специальным воском. Когда воск затвердевает и отклеивается, он оставляет отпечаток той страницы. Восковая форма равномерно покрыта очень тонким слоем порошкового графита, чтобы сделать ее проводником. Форма представляет собой катод и пластину из чистой меди в качестве анода. Два электрода погружают в ванну, содержащую раствор сульфата меди (CuSO 4 ) в качестве электролита. Когда d.c. На электроды подается питание, медь с анода переходит в раствор и осаждается на катоде i.е. восковая форма. Когда на катод (т.е. восковую форму) наносится достаточно толстый слой меди (толщиной с обычную визитную карточку), цепь отключается. Воск удаляют с катода, и на полученной медной пластине будет отпечаток страницы из меди. С этой пластины можно сделать несколько сотен тысяч отпечатков страницы.
Гальваника – Химия LibreTexts
Гальваника – это процесс нанесения одного металла на другой путем гидролиза, чаще всего в декоративных целях или для предотвращения коррозии металла.Существуют также особые виды гальваники, такие как меднение, серебряное покрытие и хромирование. Гальваника позволяет производителям использовать недорогие металлы, такие как сталь или цинк, для большей части продукта, а затем наносить различные металлы снаружи, чтобы учесть внешний вид, защиту и другие свойства, необходимые для продукта. Поверхность может быть металлической или даже пластиковой.
Введение
Иногда отделка носит исключительно декоративный характер, например, продукты, которые мы используем в помещении или в сухой среде, где они вряд ли пострадают от коррозии.На эти типы продуктов обычно наносится тонкий слой золота или серебра, что делает их привлекательными для потребителя. Гальваника широко используется в таких отраслях, как автомобилестроение, самолеты, электроника, ювелирные изделия и игрушки. В общем процессе гальваники используется электролитическая ячейка, которая заключается в нанесении отрицательного заряда на металл и погружении его в раствор, содержащий соли металла (электролиты), которые содержат положительно заряженные ионы металлов. Затем из-за отрицательного и положительного зарядов два металла притягиваются друг к другу.
Цели гальваники:
- Внешний вид
- Защита
- Особые свойства поверхности
- Технические или механические свойства
Фон
Катодом будет деталь, которую нужно покрыть, а анодом будет либо расходуемый анод, либо инертный анод, обычно либо платиновый, либо углеродный (форма графита). Иногда покрытие наносится на стеллажи или бочки для большей эффективности при нанесении покрытия на многие продукты.Пожалуйста, обратитесь к электролизу для получения дополнительной информации. На рисунке ниже ионы Ag + притягиваются к поверхности ложки, и в конечном итоге она покрывается металлическими покрытиями. В процессе используется серебро в качестве анода и винт в качестве катода. Электроны переносятся с анода на катод и проходят через раствор, содержащий серебро.
Рисунок 1 : Гальваническое нанесение серебра на ложку.
История гальваники
Гальваника была впервые открыта Луиджи Бругнателли в 1805 году с помощью процесса электроосаждения для гальваники золота.Однако его открытие не было отмечено, поскольку он был проигнорирован Французской академией наук, а также Наполеоном Бонапартом. Но пару десятилетий спустя Джону Райту удалось использовать цианистый калий в качестве электролита для золота и серебра. Он обнаружил, что цианистый калий на самом деле является эффективным электролитом. Позже в 1840 году двоюродные братья Элкингтоны использовали цианид калия в качестве электролита и сумели создать возможный метод гальваники для золота и серебра. Они получили патент на гальваническое покрытие, и этот метод получил широкое распространение по всему миру из Англии.Метод гальваники постепенно стал более эффективным и усовершенствованным за счет использования более экологичных формул и источников питания постоянного тока.
Выбор электролитов
Существует множество различных металлов, которые можно использовать для нанесения покрытия, поэтому выбор правильного электролита важен для качества покрытия. Некоторые электролиты представляют собой кислоты, основания, соли металлов или расплавленные соли. При выборе типа электролита следует помнить о некоторых вещах: коррозии, стойкости, яркости или отражательной способности, твердости, механической прочности, пластичности и износостойкости.
Подготовка поверхности
Цель подготовки поверхности перед началом наклеивания на нее другого металла – убедиться, что она чистая и не содержит загрязнений, которые могут помешать склеиванию. Загрязнение часто предотвращает отложение и отсутствие адгезии. Обычно это делается в три этапа: очистка, обработка и ополаскивание. Очистка обычно заключается в использовании определенных растворителей, таких как щелочные очистители, вода или кислотные очистители, чтобы удалить слои масла с поверхности.Обработка включает модификацию поверхности, которая заключается в упрочнении деталей и нанесении металлических слоев. Ополаскивание приводит к окончательному результату и является последним штрихом к нанесению гальванических покрытий. Двумя определенными методами подготовки поверхности являются физическая очистка и химическая очистка. Химическая очистка заключается в использовании растворителей, которые являются поверхностно-активными химическими веществами или химическими веществами, которые вступают в реакцию с металлом / поверхностью. При физической очистке применяется механическая энергия для удаления загрязнений. Физическая очистка включает абразивную чистку щеткой и ультразвуковое перемешивание.
Типы гальванических покрытий
Существуют различные процессы, с помощью которых люди могут наносить гальванические покрытия на металлы, такие как нанесение металлического покрытия массой (также гальваническое покрытие цилиндра), гальваническое покрытие на стойке, непрерывное гальваническое покрытие и нанесение покрытия на линии. Каждый процесс имеет свой собственный набор процедур, позволяющих получить идеальное покрытие.
| Массовое покрытие | Это не идеальный вариант для детализированных предметов, поскольку он неэффективен для предотвращения царапин и запутывания.Однако этот процесс эффективно обрабатывает огромное количество объектов. |
|---|---|
| Обшивка стойки | Дороже, чем массовая гальваника, но эффективен как для больших, так и для хрупких деталей. Часто детали погружены в растворы со «стойками». |
| Сплошное покрытие | Такие детали, как провода и трубки, постоянно проходят через аноды с определенной скоростью. Этот процесс немного дешевле. |
| Линия покрытия | Дешевле, так как используется меньше химикатов и используется производственная линия для штамповки деталей. |
Металлы для покрытия
Большинство гальванических покрытий можно разделить на следующие категории:
| Жертвенное покрытие | Декоративное покрытие | Функциональные покрытия | Незначительные металлы | Необычное металлическое покрытие | Покрытия из сплавов |
|---|---|---|---|---|---|
| используется в первую очередь для защиты.Металл, используемый для покрытия, жертвуется, поскольку он расходуется в реакции. К обычным металлам относятся: цинк и кадмий (сейчас запрещены во многих странах). | используется в основном в привлекательных и привлекательных целях. Обычные металлы включают: медь, никель, хром, цинк и олово. | – это покрытия, сделанные в зависимости от необходимости и функциональности металла. Обычные металлы включают: золото, серебро, платину, олово, свинец, рутений, родий, палладий, осмий и иридий. | обычно представляют собой железо, кобальт и индий, потому что их легко покрыть пластинами, но они редко используются для нанесения покрытия. | – это металлы, которые даже реже используются для гальваники, чем второстепенные металлы. К ним относятся: As, Sb, Bi, Mn, Re, Al, Zr, Ti, Hf, V, Nb, Ta, W и Mo. | Сплав – это вещество с металлическими свойствами, состоящее из двух или более элементов. Эти покрытия создаются путем нанесения двух металлов в одну ячейку. Общие комбинации включают: золото – медь – кадмий, цинк – кобальт, цинк – железо, цинк – никель, латунь (сплав меди и цинка), бронзу (медь – олово), олово – цинк, олово – никель и олово– кобальт. |
Список литературы
- Канани, Н. Гальваника: основные принципы, процессы и практика; Elsevier Advanced Technology: Oxford, UK, 2004. .
- Lowenheim, Фредерик Адольф. Современное гальваническое покрытие . 3-е изд. Нью-Йорк, Нью-Йорк: J. Wiley and Sons, 1974. .
- Блюм, Уильям и Джордж Б. Хогабум. Принципы гальваники и гальванопластики (гальванопластики) . 3-е изд. Нью-Йорк, штат Нью-Йорк: McGraw-Hill Book Company Inc., 1949.Распечатать.
- Петруччи, Ральф Х., Харвуд, Уильям С., Херринг, Ф. Г., и Мадура Джеффри Д. Общая химия: принципы и современные приложения. 9 изд. Верхняя река Сэдл: Pearson Education, Inc., 2007.
Проблемы
- Каковы цели гальваники?
- Как работает гальваника?
- Почему так важно подготовить поверхность перед нанесением гальванических покрытий?
- Какие бывают виды гальваники?
- Какие разные металлы можно использовать? (название 5)
Ответы
- Обычно гальваника используется в декоративных или функциональных целях, а также для предотвращения коррозии металла.
- Гальваника работает через электролитическую ячейку с катодом и анодом. Катод – это металл, на который необходимо нанести покрытие.
- Важно подготовить поверхность перед началом процедуры, потому что иногда на поверхности есть загрязнения, которые могут привести к плохим результатам гальваники.
- К различным типам гальванического покрытия относятся: массовое покрытие (также гальваническое покрытие цилиндра), гальваническое покрытие в стойке, непрерывное гальваническое покрытие и нанесение покрытия в линию.
- Пять металлов, которые можно использовать в гальванике: цинк, кобальт, железо, олово и платина
Авторы и авторство
- Вайшали Миттал (Калифорнийский университет в Дэвисе)
Узнайте, как гальванизировать медь
Что произошло во время процесса нанесения покрытия:
Раствор сульфата меди – это раствор электролита, который проводит электричество от одного электрода к другому, создавая электрический ток.
При протекании тока на медном аноде происходит окисление (потеря электронов), в результате чего в раствор добавляются ионы меди.
Эти ионы перемещаются по электрическому току к катоду, где происходит уменьшение (усиление электронов), осаждая ионы меди на ключ.
Ионы меди уже присутствовали в растворе сульфата меди до того, как вы начали, но реакция окисления на аноде продолжала заменять их в растворе, поскольку они наносились тонким слоем на ключ, поддерживая реакцию.
Этот проект имеет множество переменных, включая чистоту и гладкость ключа, прочность раствора сульфата меди и силу тока.
Если на ключе начинает образовываться черная, похожая на сажу субстанция, значит, вашего раствора недостаточно для протекания тока. Выньте электроды и добавьте еще медного купороса. Когда вы вставляете их обратно, убедитесь, что анод и катод находятся как можно дальше друг от друга. Обязательно делайте заметки для своего научного эксперимента, чтобы обеспечить сбор качественных данных.
Есть много проектов, которые вы можете сделать с помощью гальваники!
Одна интересная идея – использовать плоский кусок латуни в качестве катода и нарисовать на нем рисунок маркером на масляной основе. Медь не склеится там, где находится маркер.
После нанесения покрытия вы можете использовать ацетон (или жидкость для снятия лака), чтобы стереть маркер, оставив рисунок латуни, проступающий сквозь медь. Медь имеет относительно тусклый цвет, что означает, что могут потребоваться другие добавки, если требуется более яркая отделка.Если хотите, можете использовать немного полироли для металла, чтобы сделать медь блестящей.
Вы можете попробовать этот простой эксперимент с меднением, в котором не используется электролиз и требуются только бытовые материалы.
Электролиз – гальваника – серебро, анод, электроны и ионы
Другое важное применение электролитических ячеек – это гальваника серебра, золота, хрома и никеля. Гальваника производит очень тонкое покрытие из этих дорогих металлов на поверхности более дешевых металлов, чтобы придать им внешний вид и химическую стойкость, как у дорогих металлов.
При серебряном покрытии покрываемый предмет (например, ложка) изготавливается из катода электролитической ячейки. Анод представляет собой стержень из металлического серебра, а электролит (жидкость между электродами) представляет собой раствор цианида серебра AgCN в воде. Когда через элемент пропускают постоянный ток, положительные ионы серебра (Ag + ) из цианида серебра мигрируют к отрицательному аноду (ложке), где они нейтрализуются электронами и прилипают к ложке как металлическое серебро:
Между тем серебряный анодный стержень отдает электроны, превращаясь в ионы серебра:
Таким образом, анодный стержень постепенно растворяется, чтобы пополнить запасы ионов серебра в растворе.В результате металлическое серебро переместилось с анода на катод, в данном случае – на ложку. Этот процесс продолжается до тех пор, пока на ложке не будет достигнута желаемая толщина покрытия – обычно всего несколько тысячных долей дюйма – или пока серебряный слиток полностью не растворится.
При гальванике серебром цианид серебра используется в электролите, а не другие соединения серебра, такие как нитрат серебра AgNO 3 , потому что ион цианида CN – реагирует с ионом серебра Ag + , с образованием комплексного иона Ag (CN) -.Это ограничивает поступление свободных ионов Ag + в раствор, поэтому они могут осаждаться на катоде только очень постепенно. Это обеспечивает более блестящее и прочное серебряное покрытие. Золочение выполняется примерно так же, с использованием золотого анода и электролита, содержащего цианид золота, AuCN.
Книги
Чанг, Раймонд. Химия. Нью-Йорк: Макгроу-Хилл, 1991.
Шервуд, Мартин и Кристин Саттон, ред. Физический Мир. New York: Oxford, 1991.
Электролиз: Коммерческое применение электролиза
Электролизом коммерчески получают различные вещества, например хлор электролизом раствора поваренной соли; водород при электролизе воды; тяжелая вода (оксид дейтерия) для использования в ядерных реакторах, а также при электролизе воды. Металл, такой как алюминий, очищается электролизом. Раствор оксида алюминия в расплавленном минерале разлагается на чистый алюминий на катоде и на кислород на аноде.В этих примерах электроды инертны.
При гальванике металлическим покрытием обычно является анод, а наносимый объект – катод. Электролитом является раствор соли металлического покрытия. Металл покрытия осаждается на катоде, а анод пополняет запас положительных ионов, постепенно растворяясь. Электротехнические печатные формы, столовое серебро и хромированная отделка автомобилей покрываются электролизом.
Английский ученый Майкл Фарадей обнаружил, что количество материала, нанесенного на электрод, пропорционально количеству используемого электричества.Отношение количества нанесенного материала в граммах к количеству использованного электричества является электрохимическим эквивалентом материала. Фактическое потребление электроэнергии может в четыре раза превышать теоретическое потребление из-за таких факторов, как потеря тепла и нежелательные побочные реакции.


