Соединение СИП с медным кабелем
Самонесущий провод, имеющий ПЭ изоляцию и применяемый в качестве проводника энергии в воздушных и осветительных сетях с напряжением до 35 киловольт (кВ), носит название СИП. В составе его конструкции имеются фазные изолированные провода и нейтральная несущая жила. Изоляционный слой самонесущего провода сделан из полиэтилена, а сам токопроводящий материал — алюминий.
Соединение с проводкой из меди
Прямое скрепление СИП с медным кабелем невозможно, поскольку алюминиевое изделие имеет высокую степень окисляемости из-за образования пленки с повышенным сопротивлением. На медную проводку данное воздействие оказывает не очень сильное влияние, а образующаяся пленка характеризуется низким сопротивлением. Соединение напрямую через окисную пленку понижает проводимость тока, что сказывается на качестве проводки. Следовательно, для закрепления самонесущего провода с медным кабелем необходимо использовать дополнительные приспособления.
Зажимы имеют две разновидности:
- анкерные клиновые. Применяются при концевом креплении проводки, ответвленной от основной линии;
- ответвляющие. Скрепляют магистральные самонесущие провода с изолированными кабелями в ответвленных линиях.
В случае если с СИП соединяется изделие, имеющее секторы либо круглые жилы, то потребуется использование арматуры — гильз.
При соединении самонесущей проводки с медным кабелем применение гильз предполагает округление секторной жилы. Данная арматура — это алюминиевая трубка, внутри которой имеется контактная смазка. При помощи пресса с шестигранной матрицей будет происходить обжатие. Ориентироваться следует на нанесенные на гильзы зоны обжатия. Что касается изоляции, то она будет восстанавливаться термоусаживаемыми трубками с герметизирующим подслоем.
Для дополнительной защиты соединения (обязательное действие) потребуется использование кабельной термоусаживаемой перчатки, которая имеет две разновидности:
- E2R — две жилы,
- E4R — четыре жилы.
Данная перчатка имеет герметизирующий внутренний слой и защищается от УФ-излучения. Процесс соединения самонесущего провода с кабелем должен выполняться очень тщательно, чтобы места разъединения изоляции и центральный проводной элемент были под надежной защитой.
Использование термоусаживаемых муфт
Соединение может быть выполнено с применением муфт. Переходные приспособления могут использоваться для работы с имеющими пластмассовую изоляцию кабелями и применяться на воздушных линиях и на фасадах зданий. Их комплектация включает в себя:
- изоляционную перчатку,
- изоляционные термоусаживаемые трубки,
- бронированную систему заземления,
- болтовые соединители.
С использованием переходных муфт процесс соединения осуществляется по определенной системе. Предусмотрено восстановление полиэтиленового полупроводящего изоляционного слоя при помощи специальной трубки, которая выравнивает электрическое напряжение. Применяя ленту и провод-перемычку, восстанавливается кабельный экран. Далее, используется термический плавкий клей, предназначенный для герметичности муфты.
Предусмотрено восстановление полиэтиленового полупроводящего изоляционного слоя при помощи специальной трубки, которая выравнивает электрическое напряжение. Применяя ленту и провод-перемычку, восстанавливается кабельный экран. Далее, используется термический плавкий клей, предназначенный для герметичности муфты.
О переходном сопротивлении при соединении проводов
Разделы статьи:
О переходном сопротивлении при соединении проводов
Один из важнейших моментов при соединении проводов — создание наилучшего контакта. Когда мы спаиваем, скручиваем или соединяем каким-либо другим способом два провода, то получаем в результате электрический контакт. Его сопротивление в любом случае будет выше, чем у цельного провода и зависит оно от многих факторов.
Когда мы спаиваем, скручиваем или соединяем каким-либо другим способом два провода, то получаем в результате электрический контакт. Его сопротивление в любом случае будет выше, чем у цельного провода и зависит оно от многих факторов.
Более всего на переходное сопротивление влияет площадь контактируемых поверхностей. Чем она больше, тем меньше сопротивление, соответственно, тем лучше результат.
Шероховатые контакты имеют меньшую площадь, чем гладкие, поскольку при шероховатостях контакт осуществляется по микровыступам.
Величина площади зависит еще и от того, с какой силой проводники прижимаются друг к другу — чем сильнее нажатие, тем больше площадь их соприкосновения. Поэтому даже был придуман такой термин, как контактное нажатие, обозначающий силу давления одной поверхности контакта на другую. Увеличивать эту силу до бесконечности нельзя, так как можно деформировать металл контактов.
О переходном сопротивлении при соединении проводов
Сильно зависит переходное сопротивление и от такого фактора, как окисление контактов.
Пленка окиси увеличивает это сопротивление во много раз. Все мы видели, что блестящая поверхность жилы недолго остается таковой, быстро покрываясь темной пленкой.
Еще один важный момент — совместимость соединяемых проводников по электрическим и химическим свойствам. При контакте двух окислов несовместимых металлов переходное сопротивление может существенно повыситься, что ухудшает контакт.
Почему медь и алюминий напрямую лучше не соединять
Есть материалы, которые считаются электрохимическими несовместимыми — именно такова пара «медь-алюминий». Решив по-быстрому скрутить два провода из этих металлов, можно получить плачевный результат. Хотя на первый взгляд всё должно быть с точностью да наоборот — ведь электрические свойства меди и алюминия позволяют считать их лучшими из проводников, наряду с золотом и серебром. Так почему бы не соединить их?
Есть один нюанс — быстрое и весьма существенное окисление алюминиевых проводов. Медь окисляется намного меньше, пленка окиси на поверхности медного провода существенного влияния на проводимость не оказывает.
Соединение меди и алюминия образует гальваническую пару, происходит взаимное отторжение контактных поверхностей с выделением тепла и обгоранием изоляции.
Но бывают ситуации, когда соединить медный и алюминиевый провод очень нужно. Есть несколько относительно безопасных вариантов:
- использование клеммников типа «Wago»
- если на улице — возьмем ответвительные зажимы для СИП или сжимы «орешки»
- когда под рукой нет никаких специальных приспособлений, выручит обычный болт с гайкой и шайбой (ее мы проложим между медью и алюминием, исключив прямой их контакт).
Выбираем способ соединения проводов
Соединение электрических проводов может быть выполнено различными способами. Какой из них лучше выбрать, во многом зависит от величины протекающего тока и сечения провода. Немаловажно и то, из какого металла выполнены провода, одножильные они или многожильные, в каком месте будет производиться соединение и каковы условия эксплуатации.
Так, например, на улице к соединению проводов предъявляются более высокие требования, чем в помещении — атмосферные явления ухудшают качество контактных соединений. Что касается электропроводки в квартире, то способы соединения электрических проводов, применяемые лет пятьдесят назад и сейчас, существенно отличаются.
Это связано со сменой металла, из которого сделаны провода — раньше в квартирах в основном использовался алюминий, и в самых важных точках соединяли провода сваркой или опрессовкой гильзами. Это было надежно и прочно.
Теперь же первое место за проводами с медными жилами — они меньше окисляются, обладают высокой пластичностью, а соединять их предпочитают удобными и простыми в эксплуатации клеммниками.
Профессионалы обычно используют клеммные колодки, от которых можно отрезать столько гнезд, сколько нужно. Для домашнего применения весьма удобны пружинные клеммники.
По-прежнему многие используют соединение проводов скруткой, замотав ее изолентой или закрыв специальным колпачком, имеющим внутри резьбу и навинчивающимся на место соединения (СИЗ). Для прочности скрутку пропаивают или сваривают — такой контакт получается прочным и достаточно надежным.
Для прочности скрутку пропаивают или сваривают — такой контакт получается прочным и достаточно надежным.
Иногда при монтаже электропроводки требуется выполнить соединение одножильного и многожильного провода.
Простая скрутка (без пайки или сварки) в этом случае весьма нежелательна. Лучше взять клеммную колодку и с ее помощью организовать нормальный и надежный контакт. Если под рукой есть паяльник, то концы многожильных проводов все же лучше пропаять — так мы улучшим площадь контакта и предотвратим обрывание отдельных жилок.
Вне зависимости от способа соединения провода сначала надо подготовить. Для этого сначала снимаем изоляцию, а затем ножом зачищаем провод. При этом добиваемся равномерно блестящей поверхности, соскребая пленку окиси. Берем в руки паяльник.
Хоть и появилось сейчас множество новых приспособлений, предполагающих соединение проводов без пайки, но старый добрый паяльник по-прежнему частенько выручает.
Иногда мне приходится слышать, что пайка сейчас неактуальна, но это субъективное мнение, ничем серьезным не подкрепленное.
При нормальном отношении к делу получившийся контакт обладает хорошей механической прочностью и небольшим сопротивлением благодаря тому, что расплавленный припой хорошо заполняет все зазоры между соединяемыми проводами.
Основные преимущества пайки
- не требуется дорогостоящее оборудование;
- данное соединение легко поддается ремонту — достаточно лишь хорошо прогреть его тем же паяльником;
- спаянные провода могут выдержать большие нагрузки — они не раскрутятся, не переломятся и не порвутся даже при значительном механическом усилии.
Надо заметить, что пайка проводов может выполняться для соединения практически любых металлов, как одного вида, так и различных. Главная хитрость при пайке — достижение одинаковой температуры, как соединяемых поверхностей, так и припоя. Именно при соблюдении этого условия мы получим великолепный результат. Для этого надо хорошо подобрать инструмент, припой и флюс.
Это значит, что толстые скрутки 40-ваттным паяльником хорошо спаять вряд ли получится, особенно, если в помещении низкая температура воздуха.
Также можно применить особый флюс, который разъедает окись при нагреве. Главное удалить после пайки лишние остатки флюса, чтобы паяное соединение впоследствии не разрушалось. Для этого можно воспользоваться техническим спиртом или бензином «Калоша».
Место спайки надо хорошо заизолировать. Можно использовать для этого изоленту — хлопчатобумажную (более термостойкую) или виниловую (обладающую хорошей влагостойкостью). Наибольшую герметичность можно получить, проложив внутри тканевую изоляцию, а снаружи — винил. Можно вместо изоленты использовать защитный пластмассовый колпачок, который выглядит аккуратнее.
Пользуемся клеммами — быстро и удобно
Такой способ, как соединение проводов клеммами, тоже весьма неплох — ведь не зря им повсеместно пользуются опытные электрики.
Единственная проблема — пучки проводов с клеммниками не всегда получается спрятать.
Например, в стандартной распаечной коробке (80 мм) такая гирлянда может и не поместиться.
Наиболее распространены клеммные зажимы, имеющие винтовое соединение. Внутри корпуса из полиэтилена или другого изоляционного материала находятся втулки с резьбой. Винты, вкручивающиеся в резьбу, прижимают провода, которые вставляются в клеммник. Алюминий для такого соединения не очень пригоден — слишком мягкий.
Пользоваться винтовыми зажимами следует очень аккуратно — стенки латунных контактных втулок легко ломаются. И еще — при сильном затягивании контактного винта можно запросто сорвать резьбу или «слизать» паз для отвертки.
Кроме винтовых клеммников, есть еще и такие, которые для соединения используют специальные прижимные пластины. Зачищенные концы проводов вставляются между этими пластинами и прижимаются. Такой способ соединения более безопасен и меньше повреждает провода, чем предыдущий. Поэтому, если есть выбор — клеммник с винтами или с пластинами — стоит остановиться на втором варианте.
Такой способ соединения более безопасен и меньше повреждает провода, чем предыдущий. Поэтому, если есть выбор — клеммник с винтами или с пластинами — стоит остановиться на втором варианте.
Клеммники пружинные, самыми популярными из которых являются немецкие «Wago», содержащие внутри специальную антиокислительную пасту, позиционируются производителями по типу «поставил и забыл».
Если предстоит соединение проводов разного сечения или выполненных из разных материалов, такой клеммник всегда поможет. Он выдерживает ток до 32 ампер, что обычно вполне достаточно для домашнего электроснабжения. Данные клеммники являются самозажимными, поэтому ими может пользоваться даже неопытный мастер.
Как видите, скрепить между собой отдельные провода можно многими способами. В принципе, практически все они могут дать хороший результат, если выполнить операции аккуратно, соблюдая инструкции и технику безопасности. При этом браться стоит за то, что хорошо получается.
Соединение электрических проводов самозажимными клеммниками — отличный способ для тех, кто не имеет большого опыта в электрике, пайка подходит тем, у кого небольшой опыт имеется, а колодками с винтовыми зажимами лучше пользоваться профессионалам.
Поделиться статьей в социальных сетях
Оксидные пленки при коррозии металлов: Химия оксидных дефектов | Водная химия оксидов
Фильтр поиска панели навигации Oxford AcademicThe Water Chemistry of OxidesInorganic ChemistryBooksJournals Термин поиска мобильного микросайта
Закрыть
Фильтр поиска панели навигации Oxford AcademicThe Water Chemistry of OxidesInorganic ChemistryBooksJournals Термин поиска на микросайте
Расширенный поиск
Иконка Цитировать Цитировать
Разрешения
- Делиться
- Твиттер
- Подробнее
CITE
Bunker, Bruce C и William H Casey,
‘оксидные пленки в металлической коррозии: химия оксида
,
Водная химия оксидов
(
, Нью -Йорк,
2016;
онлайн-издание,
Oxford Academic
, 12 ноября 2020 г.
), https://doi.org/10.1093/oso/9780199384259.003.0019,
, по состоянию на 24 октября 2022 г.
Выберите формат Выберите format.ris (Mendeley, Papers, Zotero).enw (EndNote).bibtex (BibTex).txt (Medlars, RefWorks)
Закрыть
Фильтр поиска панели навигации Oxford AcademicThe Water Chemistry of OxidesInorganic ChemistryBooksJournals Термин поиска мобильного микросайта
Закрыть
Фильтр поиска панели навигации Oxford AcademicThe Water Chemistry of OxidesInorganic ChemistryBooksJournals Термин поиска на микросайте
Advanced Search
Abstract
Большинство металлов, используемых в нашем обществе, подвержены коррозии, от легкого потускнения серебра до зеленой патины, покрывающей наши медные статуи и электропроводку, до красной ржавчины на наших автомобилях и железных мостах (рис. 12.1, Табличка 17). Коррозия металлов часто связана с превращением металлов либо в оксиды, либо в растворимые продукты их гидролиза. Металлы, которые мы используем в наших конструкциях, а также в электронных и магнитных устройствах, разрушаются в результате этого преобразования. Было подсчитано, что ежегодные затраты на коррозию металлов для экономики США составляют сотни миллиардов долларов (5% валового национального продукта). Поэтому были предприняты огромные усилия, чтобы понять, почему металлы подвергаются коррозии, и что можно сделать для замедления процессов коррозии. Нержавеющая сталь — лишь один из примеров попыток человечества ограничить процессы коррозии. Другие примеры включают использование инертных красок на кораблях для предотвращения солевой коррозии, покрытие железа цинком для его гальванизации и использование электрохимических стратегий, таких как использование расходуемых анодов, которые подвергаются коррозии вместо железа, в качестве средства защиты более важных компонентов материалов.
12.1, Табличка 17). Коррозия металлов часто связана с превращением металлов либо в оксиды, либо в растворимые продукты их гидролиза. Металлы, которые мы используем в наших конструкциях, а также в электронных и магнитных устройствах, разрушаются в результате этого преобразования. Было подсчитано, что ежегодные затраты на коррозию металлов для экономики США составляют сотни миллиардов долларов (5% валового национального продукта). Поэтому были предприняты огромные усилия, чтобы понять, почему металлы подвергаются коррозии, и что можно сделать для замедления процессов коррозии. Нержавеющая сталь — лишь один из примеров попыток человечества ограничить процессы коррозии. Другие примеры включают использование инертных красок на кораблях для предотвращения солевой коррозии, покрытие железа цинком для его гальванизации и использование электрохимических стратегий, таких как использование расходуемых анодов, которые подвергаются коррозии вместо железа, в качестве средства защиты более важных компонентов материалов. Количество исчерпывающих текстов и обзоров о масштабах коррозии металлов с ее экономическим влиянием, по этой теме публикуется более 1000 статей в год. Тем из вас, кто заинтересован в более подробном обсуждении того, как определенные металлы подвергаются коррозии в определенных средах, таких как морская вода и кислотные дожди, следует ознакомиться с другими работами. В этой главе мы сосредоточимся на том, чтобы показать, как коррозия металлов опосредована присутствием оксидов, уделив особое внимание реакциям, протекающим в воде. В этом обзоре освещаются основные свойства оксидных пленок, которые вызывают широкий спектр сложных явлений коррозии металлов. Обсуждение основано на многих концепциях, выделенных в других главах этой книги: химия поверхности (глава 6), электрохимия (глава 11) и растворение оксидов (глава 16). Коррозия металлов часто включает электрохимические реакции, в которых металл окисляется либо водой, либо кислородом.
Количество исчерпывающих текстов и обзоров о масштабах коррозии металлов с ее экономическим влиянием, по этой теме публикуется более 1000 статей в год. Тем из вас, кто заинтересован в более подробном обсуждении того, как определенные металлы подвергаются коррозии в определенных средах, таких как морская вода и кислотные дожди, следует ознакомиться с другими работами. В этой главе мы сосредоточимся на том, чтобы показать, как коррозия металлов опосредована присутствием оксидов, уделив особое внимание реакциям, протекающим в воде. В этом обзоре освещаются основные свойства оксидных пленок, которые вызывают широкий спектр сложных явлений коррозии металлов. Обсуждение основано на многих концепциях, выделенных в других главах этой книги: химия поверхности (глава 6), электрохимия (глава 11) и растворение оксидов (глава 16). Коррозия металлов часто включает электрохимические реакции, в которых металл окисляется либо водой, либо кислородом.
Ключевые слова: Дефекты Френкеля, закон Ома, спектроскопия обратного резерфордовского рассеяния (РОР), дефект Шоттки, продукты коррозии, коэффициент диффузии, электрохимический ряд, диффузия в поле, гальваническое напряжение, генерация газообразного водорода
Предмет
Неорганическая химия
В настоящее время у вас нет доступа к этой главе.
Войти
Получить помощь с доступом
Получить помощь с доступом
Доступ для учреждений
Доступ к контенту в Oxford Academic часто предоставляется посредством институциональных подписок и покупок. Если вы являетесь членом учреждения с активной учетной записью, вы можете получить доступ к контенту одним из следующих способов:
Доступ на основе IP
Как правило, доступ предоставляется через институциональную сеть к диапазону IP-адресов. Эта аутентификация происходит автоматически, и невозможно выйти из учетной записи с IP-аутентификацией.
Войдите через свое учреждение
Выберите этот вариант, чтобы получить удаленный доступ за пределами вашего учреждения. Технология Shibboleth/Open Athens используется для обеспечения единого входа между веб-сайтом вашего учебного заведения и Oxford Academic.
- Нажмите Войти через свое учреждение.
- Выберите свое учреждение из предоставленного списка, после чего вы перейдете на веб-сайт вашего учреждения для входа.
- При посещении сайта учреждения используйте учетные данные, предоставленные вашим учреждением. Не используйте личную учетную запись Oxford Academic.
- После успешного входа вы вернетесь в Oxford Academic.
Если вашего учреждения нет в списке или вы не можете войти на веб-сайт своего учреждения, обратитесь к своему библиотекарю или администратору.
Войти с помощью читательского билета
Введите номер своего читательского билета, чтобы войти в систему. Если вы не можете войти в систему, обратитесь к своему библиотекарю.
Члены общества
Доступ члена общества к журналу достигается одним из следующих способов:
Войти через сайт сообщества
Многие общества предлагают единый вход между веб-сайтом общества и Oxford Academic. Если вы видите «Войти через сайт сообщества» на панели входа в журнале:
Если вы видите «Войти через сайт сообщества» на панели входа в журнале:
- Щелкните Войти через сайт сообщества.
- При посещении сайта общества используйте учетные данные, предоставленные этим обществом. Не используйте личную учетную запись Oxford Academic.
- После успешного входа вы вернетесь в Oxford Academic.
Если у вас нет учетной записи сообщества или вы забыли свое имя пользователя или пароль, обратитесь в свое общество.
Войти с помощью личного кабинета
Некоторые общества используют личные аккаунты Oxford Academic для предоставления доступа своим членам. Смотри ниже.
Личный кабинет
Личную учетную запись можно использовать для получения оповещений по электронной почте, сохранения результатов поиска, покупки контента и активации подписок.
Некоторые общества используют личные аккаунты Oxford Academic для предоставления доступа своим членам.
Просмотр учетных записей, вошедших в систему
Щелкните значок учетной записи в правом верхнем углу, чтобы:
- Просмотр вашей личной учетной записи и доступ к функциям управления учетной записью.
- Просмотр институциональных учетных записей, предоставляющих доступ.
Выполнен вход, но нет доступа к содержимому
Oxford Academic предлагает широкий ассортимент продукции. Подписка учреждения может не распространяться на контент, к которому вы пытаетесь получить доступ. Если вы считаете, что у вас должен быть доступ к этому контенту, обратитесь к своему библиотекарю.
Ведение счетов организаций
Для библиотекарей и администраторов ваша личная учетная запись также предоставляет доступ к управлению институциональной учетной записью. Здесь вы найдете параметры для просмотра и активации подписок, управления институциональными настройками и параметрами доступа, доступа к статистике использования и т. д.
д.
Покупка
Наши книги можно приобрести по подписке или приобрести в библиотеках и учреждениях.
Информация о покупке
| Вернуться к:
Домашняя страница энциклопедии
Содержание
Указатель авторов
Предметный указатель
Искать
Словарь
Домашняя страница ESTIR
Домашняя страница ЭКС Robert S. Alwitt Boundary Technologies, Inc. Northbrook, IL 60065-0622, USA (декабрь 2002 г.) Оксидную пленку можно вырастить на некоторых металлах — алюминии, ниобии, тантале, титане, вольфраме, цирконии — с помощью электрохимического процесса, называемого анодированием. Для каждого из этих металлов существуют технологические условия, которые способствуют росту тонкого, плотного, барьерного оксида одинаковой толщины. В ячейке для анодирования алюминиевая заготовка становится анодом, подключая ее к положительной клемме источника питания постоянного тока. Катод подключается к отрицательной клемме источника питания. Катод представляет собой пластину или стержень из углерода , свинца, никеля, нержавеющей стали любого электронного проводника, который не вступает в реакцию (инертный) в ванне анодирования. Когда цепь замыкается, электроны отрываются от металла на положительном выводе, позволяя ионам на поверхности металла вступать в реакцию с водой с образованием оксидного слоя на металле. Электроны возвращаются в ванну на катоде, где они реагируют с ионами водорода, образуя газообразный водород. (См. Приложение о химических реакциях, происходящих во время этого процесса.) Выбирают электролиты ванн, в которых оксид нерастворим или растворяется медленнее, чем осаждается, а затем растет прилипший оксидный слой. Состав ванны является основным фактором, определяющим, будет ли пленка барьерной или пористой. Барьерные оксиды
 Барьерный оксид стабилизирует поверхность от дальнейших реакций с окружающей средой и является отличным электрическим изолятором. Когда кусок алюминия, покрытый этим оксидом, используется в качестве анода в электролитической ячейке, содержащей, скажем, боратный электролит, значительный ток не течет до тех пор, пока напряжение не поднимется до 1–2 вольт. Этот оксид поддерживает электрическое поле (вольт/толщина) порядка 1 В/нм, действительно очень сильное поле. Если бы это был электронный ток, то вода окислялась бы с выделением кислорода. Но выделения кислорода не видно его не происходит, потому что оксид блокирует электроны, движущиеся в направлении от электролита к металлу. Напряжение на оксиде можно увеличивать, не вызывая протекания тока, до тех пор, пока поле в оксиде не станет достаточно большим, чтобы пропускать ионы алюминия и кислорода через оксид. Ток через оксид представляет собой ионный ток, и эти ионы вступают в реакцию, образуя оксидный слой. Процесс высокопольной ионной проводимости занимает центральное место в анодировании. Барьерный оксид стабилизирует поверхность от дальнейших реакций с окружающей средой и является отличным электрическим изолятором. Когда кусок алюминия, покрытый этим оксидом, используется в качестве анода в электролитической ячейке, содержащей, скажем, боратный электролит, значительный ток не течет до тех пор, пока напряжение не поднимется до 1–2 вольт. Этот оксид поддерживает электрическое поле (вольт/толщина) порядка 1 В/нм, действительно очень сильное поле. Если бы это был электронный ток, то вода окислялась бы с выделением кислорода. Но выделения кислорода не видно его не происходит, потому что оксид блокирует электроны, движущиеся в направлении от электролита к металлу. Напряжение на оксиде можно увеличивать, не вызывая протекания тока, до тех пор, пока поле в оксиде не станет достаточно большим, чтобы пропускать ионы алюминия и кислорода через оксид. Ток через оксид представляет собой ионный ток, и эти ионы вступают в реакцию, образуя оксидный слой. Процесс высокопольной ионной проводимости занимает центральное место в анодировании. Оксидные анионы движутся внутрь, реагируя с алюминием на границе раздела металл/оксид с образованием оксида. Катионы алюминия выходят из металла и реагируют с водой на границе раздела оксид/электролит с образованием оксида на этой поверхности. На катоде цепь завершается восстановлением ионов водорода до газообразного водорода. Новые отложения оксида на обеих границах оксида, как показано на рис. 1. (Химические реакции, происходящие во время этого процесса, см. в Приложении.) Скорость, с которой оксид загустевает, пропорциональна плотности тока (А/см 2 ). Поле в оксиде не меняется с толщиной оксида и слабо зависит от плотности тока и температуры. По мере утолщения оксида напряжение на оксиде пропорционально увеличивается, и при комнатной температуре отношение толщина/напряжение близко к 1,2 нм/В. Толщина очень однородна по всей поверхности, потому что везде падение напряжения должно быть одинаковым. Оксидные анионы движутся внутрь, реагируя с алюминием на границе раздела металл/оксид с образованием оксида. Катионы алюминия выходят из металла и реагируют с водой на границе раздела оксид/электролит с образованием оксида на этой поверхности. На катоде цепь завершается восстановлением ионов водорода до газообразного водорода. Новые отложения оксида на обеих границах оксида, как показано на рис. 1. (Химические реакции, происходящие во время этого процесса, см. в Приложении.) Скорость, с которой оксид загустевает, пропорциональна плотности тока (А/см 2 ). Поле в оксиде не меняется с толщиной оксида и слабо зависит от плотности тока и температуры. По мере утолщения оксида напряжение на оксиде пропорционально увеличивается, и при комнатной температуре отношение толщина/напряжение близко к 1,2 нм/В. Толщина очень однородна по всей поверхности, потому что везде падение напряжения должно быть одинаковым. Для каждого состава ванны и температуры существует максимальное напряжение, которое может поддерживаться до того, как произойдет пробой.  Толщина оксида составляет 220 нм, что эквивалентно 1,1 нм/В. Как и ожидалось для аморфной структуры, здесь нет отличительных структурных особенностей. Микрофотография на рис. 2 (а также на рис. 3) была получена с использованием просвечивающего электронного микроскопа, который может отображать мелкие детали при очень большом увеличении. Толщина оксида составляет 220 нм, что эквивалентно 1,1 нм/В. Как и ожидалось для аморфной структуры, здесь нет отличительных структурных особенностей. Микрофотография на рис. 2 (а также на рис. 3) была получена с использованием просвечивающего электронного микроскопа, который может отображать мелкие детали при очень большом увеличении.
 На виде сверху видна тонкая нанокристаллическая структура оксида. Кристаллиты с разной ориентацией создают характерную текстуру в поперечном сечении. Для получения такой структуры алюминий сначала нагревали до 550°С.0216 o C (1022 o F) в течение 30 секунд. Аморфный оксид, который растет во время этого кратковременного воздействия воздуха при высокой температуре, лишь немного толще, чем обычная пленка при температуре окружающей среды, но он, вероятно, содержит «зародыши» кристаллического оксида, который был идентифицирован в пленках, выращенных в течение более длительного времени при этой температуре. При последующем анодировании при 70 o C (158 o F) эти зародыши способствуют росту однородной кристаллической фазы. Для перемещения ионов алюминия и кислорода через кристаллический оксид требуется более сильное поле, чем в аморфном оксиде, поэтому более тонкий кристаллический оксид поддерживает то же напряжение, что и более толстый аморфный оксид. На виде сверху видна тонкая нанокристаллическая структура оксида. Кристаллиты с разной ориентацией создают характерную текстуру в поперечном сечении. Для получения такой структуры алюминий сначала нагревали до 550°С.0216 o C (1022 o F) в течение 30 секунд. Аморфный оксид, который растет во время этого кратковременного воздействия воздуха при высокой температуре, лишь немного толще, чем обычная пленка при температуре окружающей среды, но он, вероятно, содержит «зародыши» кристаллического оксида, который был идентифицирован в пленках, выращенных в течение более длительного времени при этой температуре. При последующем анодировании при 70 o C (158 o F) эти зародыши способствуют росту однородной кристаллической фазы. Для перемещения ионов алюминия и кислорода через кристаллический оксид требуется более сильное поле, чем в аморфном оксиде, поэтому более тонкий кристаллический оксид поддерживает то же напряжение, что и более толстый аморфный оксид. Пленка на рисунке 3 имеет толщину 125 нм, что эквивалентно 0,90 нм/В. Кристаллический оксид выгоден в качестве диэлектрика конденсатора , поскольку более тонкий диэлектрик обеспечивает более высокую емкость. Пленка на рисунке 3 имеет толщину 125 нм, что эквивалентно 0,90 нм/В. Кристаллический оксид выгоден в качестве диэлектрика конденсатора , поскольку более тонкий диэлектрик обеспечивает более высокую емкость. Пористые анодные оксиды Пористые оксиды алюминия чаще всего выращивают в разбавленной серной кислоте, обычно с концентрацией 10 весовых процентов, но также существуют промышленные процессы с использованием фосфорной кислоты, хромовой кислоты, щавелевой кислоты и смесей неорганических и органических кислот. Общей чертой этих ванн для анодирования является способность удерживать в растворе относительно высокую концентрацию алюминия. Это существенно, так как большая часть окисляющегося алюминия не удерживается в пленке, а переходит в раствор. Например, при анодировании в серной кислоте около 60 % окисленного алюминия находится в пленке, а оставшаяся часть находится в растворе. Можно легко изготовить пористые пленки толщиной 100 мкм это в 100 раз толще самой толстой барьерной пленки.
 Соотношение сторон еще более поразительное — обычно порядка 1000:1. Например, для покрытий, выращенных в серной кислоте, характерна толщина пленки от 20 до 50 мкм с порами 20 нм. Соотношение сторон еще более поразительное — обычно порядка 1000:1. Например, для покрытий, выращенных в серной кислоте, характерна толщина пленки от 20 до 50 мкм с порами 20 нм.
 В основании каждой поры находится анодный оксид толщиной 0,2 мкм, а поры разделены оксидом, входящим в состав клеточных стенок. Как показано на рисунке 7 в центре, геометрия ячейки концентрирует ток через оксид в основании поры, темно-серые зоны на рисунке. Кратчайший путь между металлом и электролитом находится в пределах этой зоны, а поле является однородным и максимальным. Это критическая особенность для развития пористой структуры. Ионы перемещаются за счет проводимости в сильном поле: катионы алюминия достигают поверхности пор и переходят в раствор, а отложение оксида ограничивается границей раздела металл/оксид в основании поры. Когда металлический алюминий окисляется, граница раздела металл/оксид перемещается в металл. Это показано на Рисунке 7 внизу, где мы пытаемся показать это внутреннее движение, накладывая друг на друга положения пор в более раннее и более позднее время анодирования. То, что было барьерным оксидом на периферии основания поры, больше не проникает в поле и становится частью клеточной стенки. В основании каждой поры находится анодный оксид толщиной 0,2 мкм, а поры разделены оксидом, входящим в состав клеточных стенок. Как показано на рисунке 7 в центре, геометрия ячейки концентрирует ток через оксид в основании поры, темно-серые зоны на рисунке. Кратчайший путь между металлом и электролитом находится в пределах этой зоны, а поле является однородным и максимальным. Это критическая особенность для развития пористой структуры. Ионы перемещаются за счет проводимости в сильном поле: катионы алюминия достигают поверхности пор и переходят в раствор, а отложение оксида ограничивается границей раздела металл/оксид в основании поры. Когда металлический алюминий окисляется, граница раздела металл/оксид перемещается в металл. Это показано на Рисунке 7 внизу, где мы пытаемся показать это внутреннее движение, накладывая друг на друга положения пор в более раннее и более позднее время анодирования. То, что было барьерным оксидом на периферии основания поры, больше не проникает в поле и становится частью клеточной стенки. Клеточная стенка и поры увеличиваются в высоту, т. е. пленка утолщается, а диаметры клеток и пор остаются фиксированными. Поскольку толщина барьерного оксида остается постоянной, напряжение и ток ячейки остаются почти постоянными по мере утолщения пленки. Клеточная стенка и поры увеличиваются в высоту, т. е. пленка утолщается, а диаметры клеток и пор остаются фиксированными. Поскольку толщина барьерного оксида остается постоянной, напряжение и ток ячейки остаются почти постоянными по мере утолщения пленки. Из этого описания стационарного роста пленки не ясно, как инициируются поры и ячейки. Металлическая поверхность имеет некоторую степень шероховатости. Это может быть процесс изготовления металла, такой как прокатка, или химическое травление, или очистка перед анодированием. Даже электрополировка, которая оставляет зеркальный блеск, создает фестончатую текстуру поверхности с мелкими ячейками диаметром порядка 100 нм. В начале роста пленка на гребнях и выступах становится толще, чем в углублениях. По-видимому, в этих местах ионы легче проходят через оксид. Это может быть из-за более высокого напряжения пленки, примесей или дефектов оксида, поэтому ток концентрируется в этих местах. Это временная ситуация, и по мере того, как оксид приобретает более однородные свойства, ток смещается в сторону более тонкого оксида в углублениях. Полезность этих пленок была бы весьма ограниченной, если бы не было возможности закрыть поры после завершения роста. Этот шаг называется «герметизация» и чаще всего выполняется путем взаимодействия анодированного покрытия с горячей водой. Оксид на поверхности и внутри пор вступает в реакцию с образованием водного оксида, имеющего другую структуру и меньшую плотность, чем анодный оксид. Из-за меньшей плотности водный оксид занимает больший объем, чем анодный оксид, из которого он образовался. Этот продукт реакции заполняет поры и образует непроницаемый анодированный слой, устойчивый в широком диапазоне атмосферных условий и условий окружающей среды. ПриложенияНиже описаны некоторые из наиболее важных приложений, а также новые приложения нанотехнологий, значение которых может возрасти. Прозрачный анодированный Чистое анодирование обычно означает анодирование серной кислотой с последующим уплотнением горячей водой. Это наиболее распространенное анодированное покрытие. Он используется на некоторых алюминиевых сплавах в качестве отделки поверхности для автомобильной отделки. Это также поверхность для коммерческих пластин для фотолитографии. Фотоэмульсия прилипает к анодированному покрытию, а печатный рисунок создается путем селективного растворения эмульсии. Печатная краска прилипает к эмульсии, а вода прилипает к открытому оксиду. Оксидная поверхность устойчива к износу и выдерживает суровые условия высокоскоростных печатных машин. Погружение анодированного покрытия в раствор красителя перед герметизацией создает привлекательную цветную поверхность для потребительских товаров. Тонкое анодированное покрытие из фосфорной кислоты используется в качестве адгезионного грунтовочного покрытия на листах из авиационных и аэрокосмических сплавов. Это отличная поверхность для эпоксидного клея, коррозионная стойкость . Анодирование хромовой кислотой используется для обеспечения оптимальной коррозионной стойкости в тяжелых условиях, таких как аэрокосмическая и военная промышленность, но поскольку хром в той или иной форме является канцерогеном, этот процесс постепенно прекращается. Архитектурные приложения Анодированный алюминий применяется в архитектуре, включая отделку дверей и окон, а также наружные структурные панели. Эти поверхности должны быть стабильными в течение многих лет в суровых атмосферных условиях. Ни прозрачные, ни окрашенные покрытия не являются удовлетворительными. Покрытия в диапазоне цветов от золотого до темной бронзы изготавливаются путем «интегрального окрашивания», которое достигается за счет использования определенных органических кислот в ванне для анодирования. Органические анионы включаются в оксид и вызывают его потемнение. Подобные оттенки получаются в результате двухэтапного процесса анодирования, в котором анодирование ацетонитом следует за этапом сернокислотного постоянного тока. На стадии переменного тока металл, обычно олово или никель, осаждается на дне пор. Металлический налет изменяет оптические свойства покрытия, а толщина металлического налета регулируется для получения желаемого цвета с помощью оптической интерференции. Эти покрытия обладают превосходной долговременной стабильностью по сравнению с цельными цветными покрытиями. Применение нанотехнологий Эти поверхности должны быть стабильными в течение многих лет в суровых атмосферных условиях. Ни прозрачные, ни окрашенные покрытия не являются удовлетворительными. Покрытия в диапазоне цветов от золотого до темной бронзы изготавливаются путем «интегрального окрашивания», которое достигается за счет использования определенных органических кислот в ванне для анодирования. Органические анионы включаются в оксид и вызывают его потемнение. Подобные оттенки получаются в результате двухэтапного процесса анодирования, в котором анодирование ацетонитом следует за этапом сернокислотного постоянного тока. На стадии переменного тока металл, обычно олово или никель, осаждается на дне пор. Металлический налет изменяет оптические свойства покрытия, а толщина металлического налета регулируется для получения желаемого цвета с помощью оптической интерференции. Эти покрытия обладают превосходной долговременной стабильностью по сравнению с цельными цветными покрытиями. Применение нанотехнологий
 Интервал признаков составлял 70-500 нм, глубина признаков составляла 200 нм, а ширина признаков была такой же величины. Эта последовательность показана на рисунке 8. В этом конкретном эксперименте анодирование в растворе щавелевой кислоты привело к образованию совершенно упорядоченных массивов пор, соответствующих узорчатой текстуре. Это показано на рисунке 9., где оксид слева рос на узорчатой поверхности, в отличие от оксида справа, который рос на поверхности без узора. Регулировка условий процесса позволяет получить точно упорядоченные массивы пор с размерами, подходящими для использования в качестве двумерных (двумерных) фотонных кристаллов в видимой области спектра. Интервал признаков составлял 70-500 нм, глубина признаков составляла 200 нм, а ширина признаков была такой же величины. Эта последовательность показана на рисунке 8. В этом конкретном эксперименте анодирование в растворе щавелевой кислоты привело к образованию совершенно упорядоченных массивов пор, соответствующих узорчатой текстуре. Это показано на рисунке 9., где оксид слева рос на узорчатой поверхности, в отличие от оксида справа, который рос на поверхности без узора. Регулировка условий процесса позволяет получить точно упорядоченные массивы пор с размерами, подходящими для использования в качестве двумерных (двумерных) фотонных кристаллов в видимой области спектра.
 Трубки изготавливаются путем покрытия стенок пор; добавление функциональных групп к внутренней стенке трубки создает трубчатые нанореакторы. Провода и трубки восстанавливаются путем растворения шаблона оксида алюминия (оксида алюминия) в реагенте, который не воздействует на наноструктуры. На рис. 10 показаны трубки из пироуглерода, созданные потоком пропилена при температуре 800°С.0216 o C (1472 o F) через пористую мембрану из оксида алюминия, отделенную от металлической подложки. Затем оксид алюминия растворяли в растворе плавиковой кислоты. Трубки изготавливаются путем покрытия стенок пор; добавление функциональных групп к внутренней стенке трубки создает трубчатые нанореакторы. Провода и трубки восстанавливаются путем растворения шаблона оксида алюминия (оксида алюминия) в реагенте, который не воздействует на наноструктуры. На рис. 10 показаны трубки из пироуглерода, созданные потоком пропилена при температуре 800°С.0216 o C (1472 o F) через пористую мембрану из оксида алюминия, отделенную от металлической подложки. Затем оксид алюминия растворяли в растворе плавиковой кислоты. Электролитические конденсаторы Основное коммерческое применение оксида анодного барьера – это диэлектрическая пленка в электролитических конденсаторах . Эти конденсаторы имеют высокую плотность энергии, широкий диапазон напряжений (от 3 до 600 вольт) и относительно низкую стоимость. Эти конденсаторы бывают двух типов: жидкостные и твердотельные. Мокрый тип использует органический электролит в качестве электрического контакта между оксидным диэлектриком и токосъемником.  Большинство алюминиевых электролитических конденсаторов относятся к этому типу и содержат рулон из двух алюминиевых фольг — одна фольга с оксидным диэлектриком — разделенных бумажной прокладкой, пропитанной органическим электролитом. В твердотельных конденсаторах используется проводящий оксид, обычно диоксид марганца, или проводящий органический полимер (например, политиофен) в качестве контакта между оксидным диэлектриком и токосъемником. В основном это танталовые конденсаторы, хотя есть некоторые алюминиевые, а в последнее время и ниобиевые конденсаторы с такой конструкцией. Для увеличения емкости на единицу объема площадь поверхности металлической подложки увеличивается перед нанесением анодного оксидного диэлектрика. Алюминиевая фольга подвергается травлению, а порошок тантала или ниобия спекается для получения гранул с большой площадью поверхности. Высокая удельная площадь, тонкий диэлектрический слой и относительно высокая диэлектрическая проницаемость (около 8 для оксида алюминия и 25 для оксида тантала) в совокупности позволяют создавать конденсаторы с более высокой плотностью энергии, чем у любого другого типа диэлектрика, такого как полимерная пленка или керамика. Большинство алюминиевых электролитических конденсаторов относятся к этому типу и содержат рулон из двух алюминиевых фольг — одна фольга с оксидным диэлектриком — разделенных бумажной прокладкой, пропитанной органическим электролитом. В твердотельных конденсаторах используется проводящий оксид, обычно диоксид марганца, или проводящий органический полимер (например, политиофен) в качестве контакта между оксидным диэлектриком и токосъемником. В основном это танталовые конденсаторы, хотя есть некоторые алюминиевые, а в последнее время и ниобиевые конденсаторы с такой конструкцией. Для увеличения емкости на единицу объема площадь поверхности металлической подложки увеличивается перед нанесением анодного оксидного диэлектрика. Алюминиевая фольга подвергается травлению, а порошок тантала или ниобия спекается для получения гранул с большой площадью поверхности. Высокая удельная площадь, тонкий диэлектрический слой и относительно высокая диэлектрическая проницаемость (около 8 для оксида алюминия и 25 для оксида тантала) в совокупности позволяют создавать конденсаторы с более высокой плотностью энергии, чем у любого другого типа диэлектрика, такого как полимерная пленка или керамика. ПриложениеКраткое описание реакций анодирования и герметизацииОбщая реакция, которая происходит во время анодирования: 2Al + 3H 2 O ==> Al 2 O 3 + 3H 2 Это сумма отдельных реакций на каждом электроде. Реакции на аноде происходят на границах раздела металл/оксид и оксид/электролит. Ионы, составляющие оксид, подвижны в условиях сильного поля. На границе раздела металл/оксид движущиеся внутрь анионы кислорода реагируют с металлом: 2Al + 3O 2- ==> Al 2 O 3 + 6e – На границе оксид/электролит движущиеся наружу катионы алюминия реагируют с водой: 2Al 3+ + 3H 2 O ==> Al 2 O 3 + 6H + (В случае растворения алюминия в электролите при образовании пористой пленки анодная реакция имеет вид: 2Al ==> 2Al 3+ + 6e – ) На катоде протекает реакция выделения водорода: 6H + + 6e – ==> 3H 2 Реакция уплотнения может быть записана как: Al 2 O 3 + 3H 2 O ==> 2AlOOH*H 2 O Связанные статьиКатодная/анодная защита от коррозииЗащита от коррозии Распределение плотности тока в гальванических элементах Электролитические конденсаторы Библиография
| |||||||||||||||||||||||||


 Толщина этого слоя и его свойства сильно различаются в зависимости от металла, и только пленки алюминия и тантала (а в последнее время и ниобия) имеют существенное коммерческое и технологическое значение в качестве конденсатора 9.0178 диэлектрики . Среди этих металлов алюминий уникален тем, что в дополнение к тонкому барьерному оксиду при анодировании алюминиевых сплавов в некоторых кислых электролитах образуется толстое оксидное покрытие с высокой плотностью микроскопических пор. Это покрытие имеет разнообразные и важные применения, включая архитектурную отделку, предотвращение коррозии автомобильных и аэрокосмических конструкций и электрическую изоляцию. На самом деле именно это пористое покрытие чаще всего считают продуктом анодирования. Поскольку на алюминии можно выращивать как барьерные, так и пористые оксиды, мы будем использовать этот металл для большинства примеров в последующем обсуждении. Те же принципы справедливы и для роста барьерного оксида на других металлах.
Толщина этого слоя и его свойства сильно различаются в зависимости от металла, и только пленки алюминия и тантала (а в последнее время и ниобия) имеют существенное коммерческое и технологическое значение в качестве конденсатора 9.0178 диэлектрики . Среди этих металлов алюминий уникален тем, что в дополнение к тонкому барьерному оксиду при анодировании алюминиевых сплавов в некоторых кислых электролитах образуется толстое оксидное покрытие с высокой плотностью микроскопических пор. Это покрытие имеет разнообразные и важные применения, включая архитектурную отделку, предотвращение коррозии автомобильных и аэрокосмических конструкций и электрическую изоляцию. На самом деле именно это пористое покрытие чаще всего считают продуктом анодирования. Поскольку на алюминии можно выращивать как барьерные, так и пористые оксиды, мы будем использовать этот металл для большинства примеров в последующем обсуждении. Те же принципы справедливы и для роста барьерного оксида на других металлах.
 Барьерный оксид растет в почти нейтральных растворах, в которых оксид алюминия трудно растворим, чаще всего в композициях бората аммония, фосфата или тартрата. Пористый оксид растет в кислых электролитах, в которых оксид может не только осаждаться, но и растворяться. Наиболее широко используемая ванна представляет собой разбавленную серную кислоту, обычно с концентрацией около 1 моля или 10 весовых процентов. Другие ванны, используемые для конкретных целей, изготавливаются из щавелевой или фосфорной кислоты.
Барьерный оксид растет в почти нейтральных растворах, в которых оксид алюминия трудно растворим, чаще всего в композициях бората аммония, фосфата или тартрата. Пористый оксид растет в кислых электролитах, в которых оксид может не только осаждаться, но и растворяться. Наиболее широко используемая ванна представляет собой разбавленную серную кислоту, обычно с концентрацией около 1 моля или 10 весовых процентов. Другие ванны, используемые для конкретных целей, изготавливаются из щавелевой или фосфорной кислоты. При пробое происходят реакции, отличные от роста оксида: выделение кислорода, окисление растворенного вещества или искрение из-за лавины электронов через оксид. Чем больше разбавлена концентрация электролита, тем выше напряжение пробоя, а максимальное напряжение, достигаемое в водных электролитах, составляет около 1000 В. При этом напряжении барьерный оксид имеет толщину около одного мкм, что в 300–500 раз толще, чем природный оксид в окружающей среде. .
При пробое происходят реакции, отличные от роста оксида: выделение кислорода, окисление растворенного вещества или искрение из-за лавины электронов через оксид. Чем больше разбавлена концентрация электролита, тем выше напряжение пробоя, а максимальное напряжение, достигаемое в водных электролитах, составляет около 1000 В. При этом напряжении барьерный оксид имеет толщину около одного мкм, что в 300–500 раз толще, чем природный оксид в окружающей среде. .  В отличие от барьерных пленок, для изготовления толстой пористой пленки не требуется высокого напряжения из-за уникальной структуры этих пленок.
В отличие от барьерных пленок, для изготовления толстой пористой пленки не требуется высокого напряжения из-за уникальной структуры этих пленок. Киотани, Л. Цай и А. Томита, Химия материалов, том 8, стр. 2109, 1996 г.) .
Киотани, Л. Цай и А. Томита, Химия материалов, том 8, стр. 2109, 1996 г.) .  Из-за развившейся вогнутой геометрии электрическое поле во впадинах несколько выше, а растворение под действием поля способствует локальному утончению оксида и концентрации тока. Это инициирует поры, а размер, плотность и распределение пор регулируются до тех пор, пока не преобладает стационарное состояние. Для коммерческих процессов большая часть корректировки обычно происходит в течение первой минуты.
Из-за развившейся вогнутой геометрии электрическое поле во впадинах несколько выше, а растворение под действием поля способствует локальному утончению оксида и концентрации тока. Это инициирует поры, а размер, плотность и распределение пор регулируются до тех пор, пока не преобладает стационарное состояние. Для коммерческих процессов большая часть корректировки обычно происходит в течение первой минуты. (См. Приложение о химической реакции, происходящей во время герметизации.)
(См. Приложение о химической реакции, происходящей во время герметизации.) 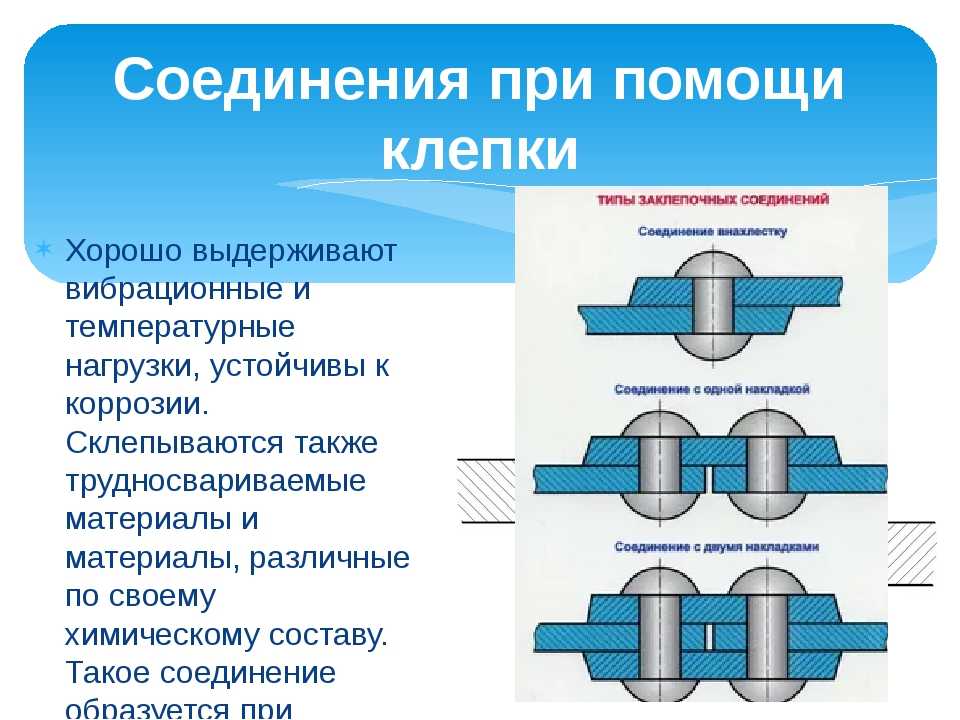
 8. Процесс изготовления идеально упорядоченного пористого оксида. Черная структура представляет собой форму SiC (карбид кремния), используемую для создания упорядоченного массива выпуклых углублений на поверхности алюминия перед анодированием (из Asoh et al., см. Библиографию).
8. Процесс изготовления идеально упорядоченного пористого оксида. Черная структура представляет собой форму SiC (карбид кремния), используемую для создания упорядоченного массива выпуклых углублений на поверхности алюминия перед анодированием (из Asoh et al., см. Библиографию).  Uchi, T. Kanno, and RS Alwitt, “Journal of The Electrochemical Society” Vol. 148, стр B17-B23, 2001.
Uchi, T. Kanno, and RS Alwitt, “Journal of The Electrochemical Society” Vol. 148, стр B17-B23, 2001.
